在日常生活中,人们常常“谈癌色变”,对于科研工作者来说,也是深感无力,因为肿瘤细胞几乎不可控。
随着对细胞死亡研究的不断深入,科学家们发现了一种新的细胞死亡方式--铁死亡。由于铁死亡的激活可导致肿瘤细胞的死亡,因此这种受调控的细胞死亡方式使得治疗癌症成为可能。
还记得吗?半年前小编曾以两篇高分文章为例,带着大家领略了一下铁死亡的研究思路:
第一篇是关于p53能够通过SLC7A11调节胱氨酸代谢,调控ROS应答并通过铁死亡抑制肿瘤生长;第二篇则是关于能量胁迫可以激活AMPK激活,从而抑制ACC并降低花生四烯酸的合成,最终抑制铁死亡。
原文链接:https://mp.weixin.qq.com/s/LNrR3Hs7W9e6eobttR8Okw
鉴于铁死亡热度如同这火热夏季一般持续不减,小优也是在持续关注,在查阅文献中发现一篇53分的高分文章,忍不住要拿出来与大家分享一番。内容较多,干货满满,必要时请收藏保存。

文如其名,属实可以让我们“大开眼界”!文章主要介绍了铁死亡的关键分子机制,描述了铁死亡与肿瘤相关信号通路之间的串扰,并讨论了铁死亡在全身治疗、放射治疗和免疫治疗中的潜在应用。
那么为了方便大家快速阅读文章,小编也整理出了文章的核心观点:
1.铁死亡是一种调控细胞死亡的形式,主要依赖于铁介导的氧化损伤和随后的细胞膜损伤。
2.铁死亡可通过两种主要途径引起:外源性/转运体依赖途径,以及内源性/酶调节途径。
3.铁积累的增加,自由基的生产,脂肪酸供应和脂质过氧化的专用酶是诱导铁死亡的关键。
4.多个氧化和抗氧化系统,与自噬和膜修复机制共同作用,形成了铁死亡中脂质过氧化的过程。
5.在形成肿瘤的过程中中,铁死亡在肿瘤促进和抑制中具有双重作用,这取决于损伤相关分子模式的释放和肿瘤微环境中铁死亡损伤引发的免疫反应的激活。
6.铁死亡影响化疗、放疗和免疫治疗的疗效,因此联合靶向铁死亡信号的药物可以改善铁死亡这些治疗的结果。
好嘞,相信大家浏览完上述内容,已经对文章大意有所了解,接下来让我们细细研磨这篇文章的精华,感受高分文章的魅力所在吧!
首先,我们需要了解什么是铁死亡?
铁死亡是铁依赖性的、非细胞凋亡性的细胞死亡形式。它主要是细胞内脂质活性氧(ROS)生成与降解的平衡失调所致,当细胞抗氧化能力降低,脂质活性氧堆积,就能引起细胞氧化性死亡,即铁死亡。
铁死亡可以通过外部或内在的途径被引发。外部途径是通过抑制细胞膜转运体如胱氨酸/谷氨酸转运体(也称为XC-系统)或通过激活血清转铁蛋白和乳转铁蛋白来启动的。内部途径通过细胞内抗氧化酶(如谷胱甘肽过氧化物酶GPX4)的阻断而被激活。

图1 铁死亡的分子机制
以抑制铁死亡通路为例。胱氨酸(Cys2)经XC-系统进入细胞,然后被氧化成半胱氨酸(Cys),Cys用于谷氨酸-半胱氨酸连接酶(GCL)和谷胱甘肽合成酶(GSS)催化合成谷胱甘肽(GSH)的反应。GPX4利用GSH作为还原辅助因子,能够将脂氢过氧化物还原为脂醇。GSH-GPX4抗氧化系统在保护细胞免于铁死亡中起着重要作用。AIFM2-CoQ10、ESCRT-III膜修复和GCH1-BH4体系也能抑制铁死亡。
一、铁死亡的氧化损伤
铁积累和脂质过氧化是在铁死亡过程中引发膜氧化损伤的两个关键信号。铁死亡的核心分子机制涉及调节氧化损伤和抗氧化防御之间的平衡。
在动物模型中,由于多个水平的干预(如增加铁吸收、减少铁储存和限制铁外流)导致铁增加,通过完整信号通路促进了铁死亡。
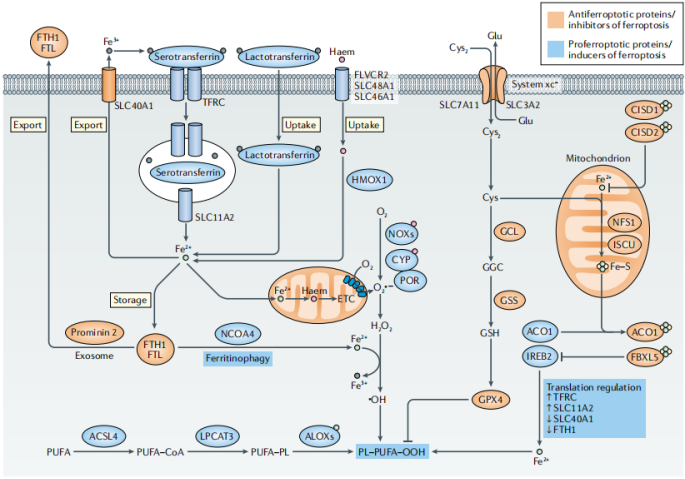
图2:铁死亡中的铁代谢
载铁的血清转铁蛋白-转铁蛋白受体(TFRC)复合物通过核内体内化,通过自然抗性相关巨噬细胞蛋白(SLC11A2)释放铁(Fe2+)到细胞质中。乳转铁蛋白和血红素通过细胞膜中不同的摄取途径提供额外的铁来源。Fe2+主要通过细胞膜上的溶质载体家族(SLC40A1)输出,但也可以通过外泌体作为铁蛋白输出。铁死亡在翻译水平上受铁调节蛋白(IRPs) ACO1和IREB2的调控。
在铁死亡中,多不饱和脂肪酸(PUFAs),特别是花生四烯酸和肾上腺酸,最容易发生过氧化反应,从而导致脂质双分子层的破坏,影响膜功能。细胞膜中PUFAs的生物合成和重构需要ACSL4和LPCAT3酶。ACSL3将单不饱和脂肪酸(MUFAs)转化为酰基辅酶A酯,并与膜磷脂结合,从而保护癌细胞免受铁死亡。AMPK介导的beclin 1磷酸化通过抑制还原谷胱甘肽(GSH)的产生来促进铁死亡,而AMPK介导的ACAC磷酸化被认为通过限制PUFA的产生来抑制铁死亡。
了解了一些促进和抑制铁死亡的的分子机制,相信大家已经有所收获了,接来下作者就铁死亡在癌症中的相关通路做了详细总结。
二、铁死亡中癌症相关通路
RAS
RAS家族的致癌基因(HRAS、NRAS和KRAS)是所有人类癌症中最常见的突变基因。Sotorasib是一种KRAS-G12C突变蛋白的直接抑制剂,在NSCLC73患者中具有很好的活性,另一种选择性抑制剂Adagrasib也显示出较好的临床活性。RAS或其下游信号分子(BRAF、MEK和ERK)的基因或药理性的抑制作用逆转Erastin和RSL3的抗癌活性,可能是因为RAS基因突变信号通过调节铁代谢相关基因的表达,如TFRC、FTH1、FTL丰富了细胞的铁水平。这些临床前研究结果支持了我们的观点,即诱导铁死亡可能构成一种适合的策略来对抗致癌的载RAS肿瘤。
TP53
一些代谢相关基因,如SAT1、FDXR88和GLS2在各种条件下都被报道为p53介导的铁死亡的直接靶点。p53可以通过直接结合二肽基肽酶DPP4来抑制人结直肠癌(CRC)细胞中NOX介导的脂质过氧化或通过诱导纤维肉瘤细胞中CDKN1A的表达来限制铁死亡。
p53的表达增加了erastin诱导的ROS生成,部分依赖于SCL7A11表达降低:
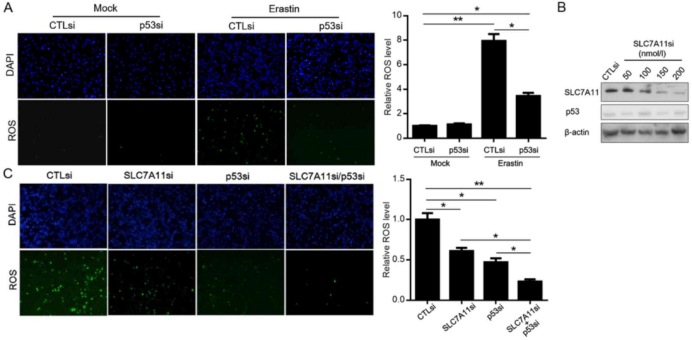
图3
(与图4皆引自Upregulation and activation of p53 by erastininduced reactive oxygen species contribute tocytotoxic and cytostatic effects in A549 lung cancer cells)
以在A549细胞中的实验为例,结果表明:
3A:A549-p53si细胞中的ROS水平低于A549-CTLsi细胞中的ROS水平
3B:SCL7A11si有效敲低SCL7A11的表达,而又不干扰p53的表达
3C:单敲低和共敲低均能抑制ROS,p53可能通过抑制SCL7A11而部分诱导了ROS的产生
Erastin诱导p53表达对A549细胞产生细胞毒作用,导致铁死亡和凋亡:

图4
结果表明:
图4A.B:erastin可以有效抑制A549细胞的存活。Si-p53减弱了erastin的细胞毒性。
通过检测caspase-3活性而确认的凋亡(图4C),p53的敲低抑制了erastin诱导的细胞死亡,如CFSE / PI双重染色(图4D)。
通过在不干扰caspase-3活性的情况下抑制细胞铁死亡(图4E),p53敲低也抑制erastin诱导的凋亡作用(图4F.G)
迄今发表的数据不仅表明脂质过氧化是铁死亡的一个关键因素,而且还表明铁死亡的单个p53靶基因或结合蛋白在整体中的重要性可能是细胞类型特异性的。
NFE2L2
临床前研究表明,NFE2L2信号转导是抗铁死亡的重要防御机制,并参与了Sorafenib在HCC细胞中的导入。NFE2L2通过反式激活几个与铁代谢、GSH代谢和ROS解毒酶有关的细胞保护基因来限制铁死亡中的氧化损伤。NFE2L2的功能增益突变或KEAP1的功能缺失突变进一步增加了氧化应激反应的复杂性,这反过来可能影响对铁死亡的抗性。

图5:KEAP1的蛋白质结构域
(与图6皆引自NRF2 and the Hallmarks of Cancer)
KEAP1由一个N端结构域(NTR)、一个Broad-Complex、轨道、bric-à-brac (BTB)结构域、一个干预区(IVR)和六个与C端结构域(CTR)结合的Kelch结构域组成,这些结构域与NRF2、p62和其他E/ STGE蛋白相互作用。BTB结构域对于KEAP1二聚和与CUL3的相互作用非常重要,它包含一个半胱氨酸残基(C151),可以感知活性氧(ROS)和亲电试剂。位于其他KEAP1结构域的其他半胱氨酸残基对其他刺激有响应(未显示)。
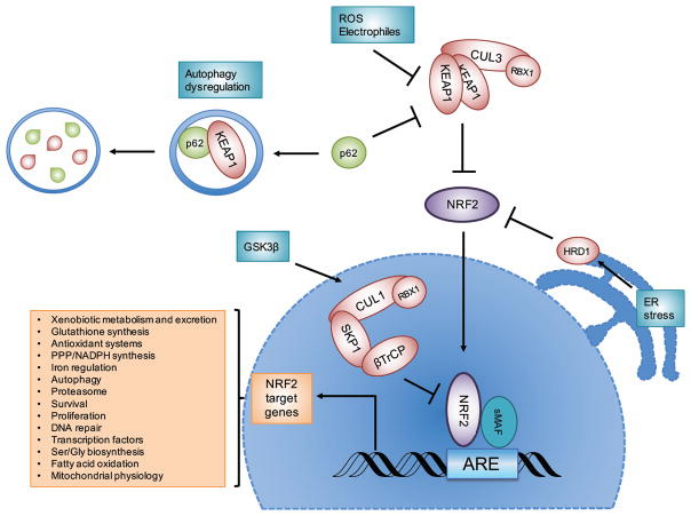
图6:NRF2的信号通路
NRF2受E3泛素连接酶复合物的负调控:KEAP1-CUL3-RBX1复合物、β-TrCP-SKP1-CUL1-RBX1复合物和HRD1。当NRF2蛋白在暴露于活性氧(ROS)、亲电试剂或自噬异常调节后而升高时,NRF2会转位到细胞核,与sMAF蛋白二聚,并与抗氧化反应元件(ARE)结合,激活其靶基因的转录。图6指出了NRF2靶基因调控的一般过程的例子。
HIF
在HT-1080纤维肉瘤细胞中,缺氧诱导表达的HIF1α通过增加脂肪酸结合蛋白3和7的表达来抑制铁死亡,从而促进摄取脂肪酸和增加储存脂质的能力,避免随后的脂质过氧化。相反,在RCC来源的细胞中,EPAS1的激活通过上调HILPDA的表达来促进铁死亡,从而增加PUFA的产生和随后的脂质过氧化。因此,有效控制HIF介导的信号对维持脂质稳态以形成铁死亡性反应是必要的。

图7:EGLN2介导的HIF1A下调促进了铁死亡
(引自Clockophagy is a novel selective autophagy process favoring ferroptosis)
7A:用RSL3 (0.5 μM)处理HT1080和Calu-1细胞12小时后,对内参和EGLN2敲除(EGLN2KD) HT1080和Calu-1细胞中的指示蛋白进行Western blot分析。
7B :Western blot检测HT1080和Calu-1细胞中RSL3 (0.5 μM)在无adaptaquin (4 μM)作用12小时后的表达情况。
7C.D :RSL3 (0.5 μM)在没有或有chetomin (0.25 μM)和KC7F2 (25 μM)作用12小时后的MDA水平(C)和细胞死亡(D)分析(n = 3,*P < 0.05)。
7E:在缺氧(1% O2)处理24小时后,对HIF1A敲低(HIF1AKD) HT1080和Calu-1细胞中指示蛋白做Western blot分析对照。
7F~I:分析MDA水平(F),细胞死亡(G),脂滴(H)和基因mRNA (I)表示的在缺氧(1% O2, 24小时)预处理后进行在RSL3(0.5μM), FIN56(5μM) 12小时(n = 3 * P < 0.05)条件下HT1080和Calu-1细胞培养。
结果表明:
- 在EGLN2下调或过表达artnl的HT1080细胞中,使用HIF1A抑制剂(例如,chetomin和KC7F2)或敲除HIF1A可恢复RSL3诱导的MDA生成(图7C)和细胞死亡(图7D)。
- 缺氧预处理诱导了hif1a的表达(图7E)。
- 脂滴的形成,在RSL3和FIN56的响应下,通过缺氧诱导的HIF1A激活得以恢复(图7H)。
综上所述,这些发现证实了HIF1A是铁死亡的促存活因子,而EGLN2介导的HIF1A下调促进了铁死亡。
EMT
LYRIC蛋白(又称异粘蛋白)是EMT的正调节器,通过抑制GPX4和SLC3A2的表达来促进铁死亡。CD44依赖的铁内吞作用增加促进铁依赖的去甲基化酶的活性,促进与EMT信号相关的基因的表达,从而使乳腺癌细胞对铁死亡敏感。这些临床前研究的数据表明,EMT可能会导致对基于铁死亡的治疗的易感性。
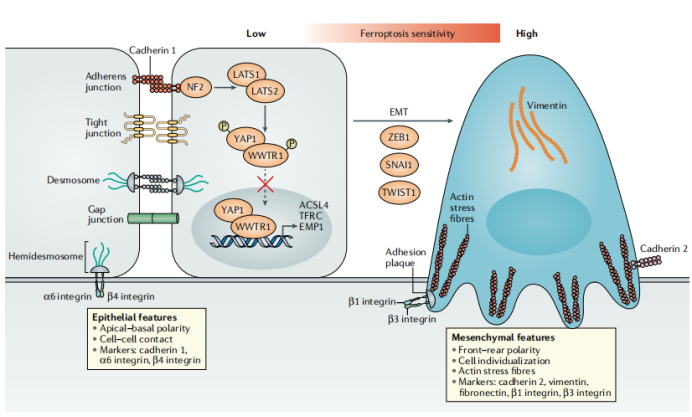
图8:EMT在铁死亡中的作用
在上皮细胞中,细胞-细胞接触抑制铁死亡,部分是通过钙粘蛋白1介导的抑制YAP1转录活性。相比之下,间充质状态的细胞由于细胞-细胞接触的缺失和参与上皮-间充质转化(EMT)的因子的激活,如ZEB1、SNAI1和TWIST1,容易发生铁死亡。
那么哪些药物可能是通过铁死亡的途径来治疗肿瘤呢?它的作用机理是什么呢?作者下文也展开了探讨。
三、肿瘤治疗中的铁死亡
系统治疗
传统的细胞毒性和靶向药物通过多种机制发挥作用,其总体目标是通过诱导癌细胞死亡而不影响未转化细胞来减缓或阻止肿瘤生长。 越来越多的临床前证据表明,诱导铁死亡可能是一种有用的治疗策略,可预防对多种癌症疗法(如拉帕替尼、厄洛替尼、曲美替尼、达拉非尼和威罗菲尼)的获得性耐药。
|
索拉非尼(Sorafenib) |
1. 索拉非尼是第一个被批准用于治疗不能切除的肝癌、晚期肾癌和分化型甲状腺癌的多酪氨酸激酶抑制剂; 2. 索拉非尼抑制多种细胞内激酶(RAF、野生型和突变型 BRAF)和细胞表面激酶(KIT、FLT3、RET、VEGFR1-3 和 PDGFRB); 3.索拉非尼通过靶向激酶(RAF,KIT,BET等)诱导前列腺癌细胞或肝癌细胞的凋亡和自噬; 4.索拉非尼通过抑制XC-系统的活性来诱导铁死亡。 5.在临床环境中,铁死亡和/或细胞凋亡对索拉非尼抗癌活性的贡献程度仍不清楚。 |
|
柳氮磺吡啶(Sulfasalazine) |
1.柳氮磺吡啶及其代谢物的作用机制可能与淋巴细胞抑制作用和白细胞调节作用有关; 2.除了抗炎活性,柳氮磺吡啶还可以通过抑制xc -系统来抑制淋巴瘤和其他癌细胞的生长。 |
|
他汀类药物(Statins) |
1.通过减少甲羟戊酸途径中异戊烯焦磷酸的产生,他汀类药物能够抑制硒蛋白(如GPX4)和辅酶Q10的生物合成,从而促使铁死亡或选择性诱导间充质细胞的调节性细胞死亡。 2.那些调控铁死亡的胆固醇调节基因和蛋白表达水平的有关信息可能有助于确定最有可能对他汀类药物有临床反应的患者。 |
|
青蒿素(Artemisinins) |
除了诱导细胞凋亡,青蒿素(尤其是青蒿琥酯和双氢青蒿素)还可以通过促进铁蛋白吞噬从而增加细胞内游离铁水平,从而引发癌细胞的铁死亡。 |
|
胱/半胱氨酸酶 (Cyst(e)inase) |
1.Cyst(e)inase可以有效降解小鼠和食蟹猴血清中的半胱氨酸和胱氨酸; 2.使用胱氨酸酶调节细胞外胱氨酸水平的策略可以为基于铁死亡的抗癌疗法开辟新的治疗机会,特别是与ROS诱导药物(如阿霉素、吉西他滨、紫杉醇、5-氟尿嘧啶、硼替佐米和三氧化二砷)联合使用时。 |
免疫疗法
免疫检查点抑制剂(ICIs)主要通过激活有效的细胞毒性T细胞驱动的抗肿瘤免疫反应来发挥作用,而细胞毒性T细胞驱动的免疫可诱导癌细胞中的铁死亡(图9)。
a.IFN-γ诱导死亡的活性 b.TGFβ1诱导铁死亡的活性 c.铁死亡的免疫调节作用
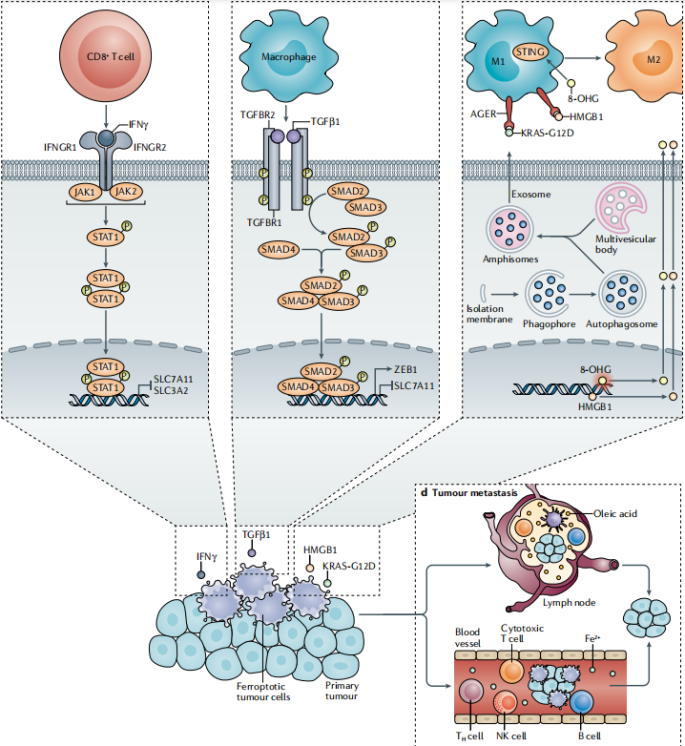
图9:铁死亡在肿瘤免疫中的作用
- CD8+T细胞释放的IFN-γ通过激活JAK1-STAT1信号通路诱导肿瘤细胞铁死亡,JAK1-STAT1信号通路转录调控SLC7A11和4F2细胞表面抗原重链(SLC3A2)的表达。
- 许多类型的细胞(如巨噬细胞)释放的TGFβ1通过SMAD蛋白介导的信号激活促进肿瘤细胞铁死亡,从而转录调控靶基因的表达。
- 铁性肿瘤细胞释放损伤相关分子模式(DAMPs),如高迁移率族蛋白B1(HMGB1)、KRAS-G12D和8-羟基鸟苷(8-OHG),影响肿瘤微环境中固有免疫细胞(如巨噬细胞)的功能。
- 淋巴组织中的肿瘤细胞,如转移性黑色素瘤细胞,脂质过氧化水平较低,因此限制了铁死亡,并比在血液中具有更高的转移潜能。
放疗
放疗主要诱导DNA损伤下游细胞的凋亡。ATM介导的SLC7A11下调与放疗诱导的癌细胞中铁死亡有关,而在皮下肿瘤模型中,放疗联合ICIs会使这种抗癌作用增强。除了下调SLC7A11,放疗还上调ACSL4,从而增加脂质合成和随后的氧化损伤,从而诱导铁死亡。
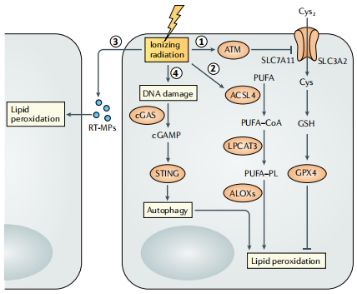
图10:铁死亡在放射治疗中的作用
放疗可通过多种机制引起癌细胞的铁死亡。抑制SLC7A11激活ACSL4的表达,从而促进PUFAs插入到膜磷脂中,形成含多不饱和脂肪酸的磷脂(PUFA-PLs),用于随后的脂氧合酶介导的氧化。受辐射的肿瘤细胞释放的微粒(RT-MPs)主要通过铁死亡来产生,这种微粒可诱导旁效应。环状GMP-AMP合成酶(cGAS)的激活信号诱导自噬依赖的铁死亡。
纳米疗法
使用携带化学物质或生物材料的纳米粒子将为提高现有的铁死亡诱导剂的疗效以及开发治疗癌症的新诱导剂提供可能性。例如,铁死亡诱导剂醉茄素A在水中溶解度较差,对小鼠有毒性。如果使用两亲性可降解的PH敏感纳米载体给药,可避免这种不利的药物学特征。然而,纳米颗粒对人类健康的长期影响仍需仔细评估。
四、挑战与看法
靶向调控肿瘤细胞中铁死亡的途径是一种新兴的抗癌策略。尽管对铁死亡的研究迅速发展,但在文末作者仍提出了几个有待解决的挑战。
1.脂质过氧化对于铁死亡至关重要,但细胞毒性是由该反应本身的产物介导的,还是需要脂质过氧化下游的信号分子介导的,仍有待确定。作者认为,可能是与未知蛋白形成的加合物导致细胞膜透孔的形成,介导了脂质过氧化的致死效应。
2.肿瘤细胞(包括癌症干细胞)的代谢重编程是如何与癌细胞特异性的铁死亡性反应相结合的尚不清楚。
3.铁死亡激活物可引起骨髓损伤。降低促进铁死亡药物的毒性或脱靶效应仍然是一个挑战。
4.为了最大限度地提高预铁死亡症治疗的疗效,对肿瘤细胞适应和产生耐药性的机制还需更全面的了解。
5.如何识别对促铁死亡症治疗反应的生物标志物?尽管它们的临床意义尚不清楚,但确定与反应性相关的生物标志物,对制定治疗计划有帮助!
呼,终于快要结束了,小编也累得够呛,不过能够跟大家分享这些前沿的知识,小编也是非常高兴的鸭!
虽然这篇综述结束了,但是相信大家都受益匪浅。身为优宁维小编,也真心地希望我们的解读分享能够帮助到大家,毕竟未来还是需要众位科研工作者同心勠力来创造的,相信我们优宁维能够助力各位乘风破浪,加油!
本文涉及相关产品
|
货号 |
产品名称 |
|
Ferroptosis Antibody Sampler Kit(检测指标:GPX4、NCOA4、KEAP1、NRF2、4F2hc/CD98、FTH1、xCT/SLC7A11、DMT1/SLC11A2) |
|
|
Phospho-FLT3 (Tyr842) (10A8) Rabbit mAb |
|
|
CD71 (D7G9X) XP® Rabbit mAb |
|
|
Axl (C89E7) Rabbit mAb |
|
|
DPP4/CD26 (D6D8K) Rabbit mAb |
|
|
IFN-γ (D3H2) XP® Rabbit mAb |
|
|
p53 Antibody Sampler Kit |
|
|
TGF-β Receptor II (E5M6F) Rabbit mAb |
|
|
CCK-8试剂盒 |
|
|
MTT细胞增殖及细胞毒性检测试剂盒 |
|
|
Iron Microplate Assay Kit |
|
|
Total Iron-binding Capacity Microplate Assay Kit |
|
FSP1和GPX4抑制剂药物筛选试剂盒 |
性能 |
|
|
FSP1 Fluorescent Inhibitor Screening Assay Kit |
包括人重组蛋白FSP1、阳对抑制剂iFSP1,可以分析45个样品(一个复孔)或29个样品(两个复孔) |
|
|
GPX4 Inhibitor Screening Assay Kit |
包括人重组蛋白GPX4、阳对抑制剂ML-162,可以分析45个样品(一个复孔)或29个样品(两个复孔) |
|
好消息
CST为科研助力,细胞生物学抗体系列促销来袭!
凡是促销活动期间购买细胞生物学相关抗体即可获得环保清新马克杯
小优准备好了,等你来寻!
促销详情及促销产品列表请点击上图 ▲








