引言
在生物医学领域,可植入生物材料和生物医学器件的广泛应用为提高人类健康水平做出了巨大贡献。然而,这些材料在植入后往往会引起异物反应(Foreign Body Response, FBR),这不仅影响材料的功能,还可能导致器件失效,给患者带来极大的困扰。针对这一问题,研究者们长期以来致力于开发具有良好生物相容性的表面涂层,以期降低FBR。然而,传统涂层方法面临着多种挑战,如材料稀缺、工艺复杂、涂层不均匀和涂层脱落等。为了克服这些难题,浙江大学高分子科学与工程学系的张鹏研究员团队近日在《自然·通讯》(Nature Communications)上发表了一项重大突破性研究,成功开发出一种无需涂层的免疫相容性弹性体——EVADE弹性体。这一创新成果有望为可植入医疗器械的免疫相容性材料提供全新的选择。

一、研究背景
- 可植入生物材料的挑战
可植入生物材料广泛应用于医学领域,如人工关节、心脏起搏器、导管等。然而,这些材料在植入后,会引起人体的异物反应,表现为炎症和纤维囊的形成。这些反应会严重影响材料的功能,甚至导致器件失效。对于弹性体基材来说,目前广泛接受的方法是开发生物相容性表面涂层。然而,这种涂层方法仍然面临着一系列挑战,如材料稀缺、涂层工艺复杂、涂层不均匀和涂层脱落等。
- 传统涂层方法的局限性
传统涂层方法主要是通过将生物相容性材料涂覆在弹性体表面,以降低FBR。然而,这种方法在实际应用中遇到了许多困难。首先,具有持久抗异物反应性能的材料稀缺,使得涂层材料的选择受限。其次,涂层工艺复杂,不适合大规模工业生产。再者,涂层应用不均匀,容易导致覆盖不足,影响效果。最后,在复杂的生理环境中,涂层容易脱落,失去保护作用。

二、EVADE弹性体的开发
- EVADE弹性体的设计
为了克服传统涂层方法的局限性,张鹏研究员团队开发出了一种无需涂层的免疫相容性弹性体——EVADE弹性体。EVADE材料基于四氢吡喃醚衍生的甲基丙烯酸酯免疫调节单体HPEMA。该单体易于合成,并能通过自由基聚合反应实现聚合。为了在聚合物结构中引入物理可交联的部分,研究者将HPEMA与丙烯酸十八酯(ODA)共聚。ODA具有长烷基链,可以在共聚物中形成微晶,从而实现物理交联。通过本体聚合制备的共聚物,以HPEMA的摩尔分数命名,如由90 mol% HPEMA和10 mol% ODA组成的共聚物被命名为H90。
- EVADE弹性体的性能评估
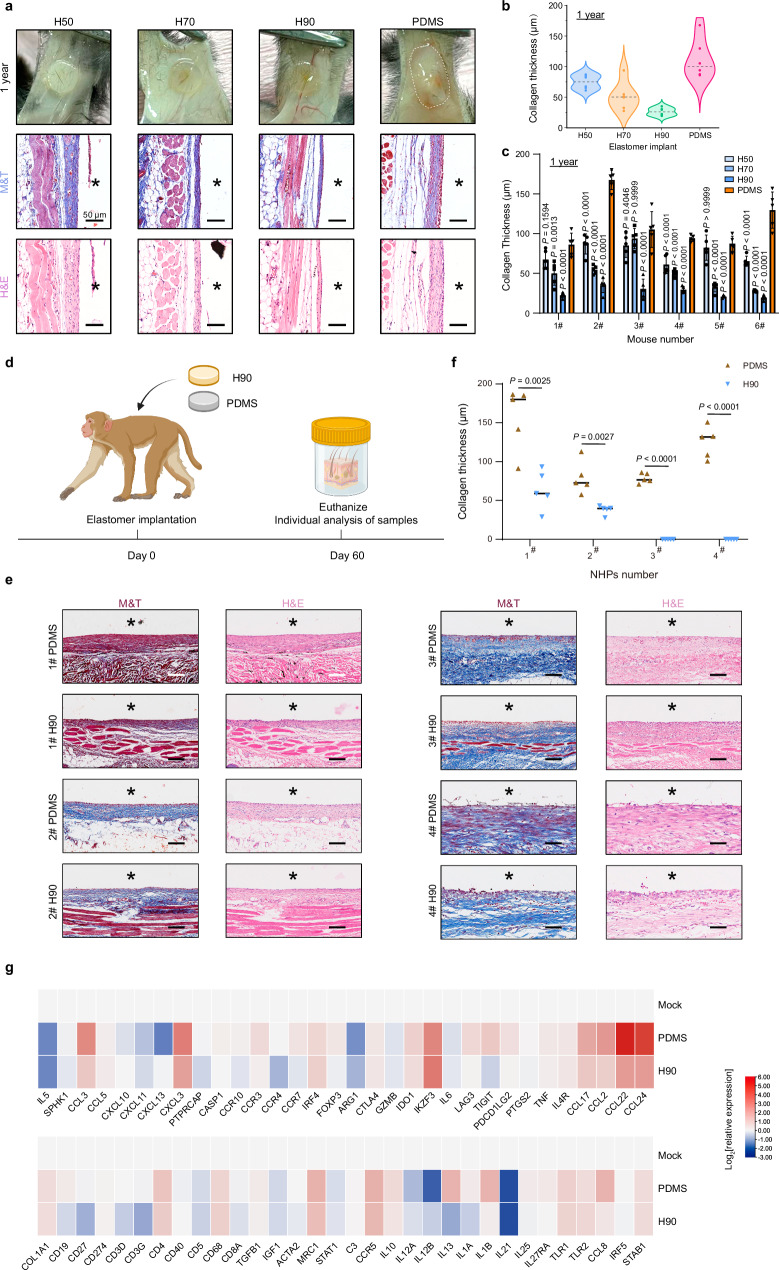
为了评估EVADE弹性体的性能,研究者进行了一系列体内和体外实验。首先,他们选择了三个样品H50、H70和H90,进行进一步的体内植入测试,以评估它们的纤维化反应。实验结果表明,EVADE材料(特别是H90)在小鼠皮下植入一个月后,形成的纤维化囊厚度显著低于常用医用弹性体PDMS。此外,研究者还将H90与其他四种常用的生物医用可植入聚合物进行比较,包括乙烯-甲基丙烯酸酯共聚物(EMA)、热塑性聚氨酯(TPU)、聚烯烃弹性体(POE)和聚酰胺(PA)。实验结果显示,植入H90后几乎未形成任何纤维囊,而其他所有材料均形成了较厚的纤维化包膜。这表明EVADE材料具有优异的免疫相容性。
除了纤维化反应评估外,研究者还研究了EVADE材料在小鼠皮下植入两周后引发的急性炎症反应。实验结果表明,H90仅引起非常微弱的炎症反应。通过免疫组织化学切片分析和单细胞RNA测序(scRNA-seq)分析,研究者发现H90的植入引发了免疫细胞中炎性细胞因子、趋化因子和集落刺激因子的广泛下调。
三、EVADE弹性体的抗异物反应机制
- 抑制纤维化反应的新靶点
为了深入探讨EVADE弹性体的抗异物反应机制,研究者进行了蛋白质组学分析。实验结果显示,在植入后24小时内,白蛋白是PDMS和H90材料表面吸附量最大的蛋白质。然而,在PDMS表面,炎症相关蛋白S100A8和S100A9的比例较高,而在H90表面的吸附量则显著较低。这些结果表明,S100A8/A9蛋白的表达和吸附可能会加剧炎症反应,进而促进体内FBR的发生。为了验证这一假设,研究者构建了S100A9药物抑制模型和S100A8基因敲除模型,并进行了纤维化反应评估。实验结果显示,抑制S100A8/A9表达可以显著降低植入物的异物反应。这表明S100A8/A9蛋白在材料植入后的纤维化过程中起着关键作用,降低这些蛋白的表达可以有效减轻材料诱导的异物反应。
- 调节免疫反应
除了抑制纤维化反应外,EVADE弹性体还能调节植入后引发的先天性和适应性免疫反应。通过免疫组织化学切片分析和scRNA-seq分析,研究者发现H90的植入显著降低了邻近组织中与炎症相关的蛋白质S100A8/A9的表达,并引发了免疫细胞中炎性细胞因子、趋化因子和集落刺激因子的广泛下调。这些结果表明,EVADE弹性体通过调节免疫反应来降低FBR。
四、EVADE弹性体的实际应用
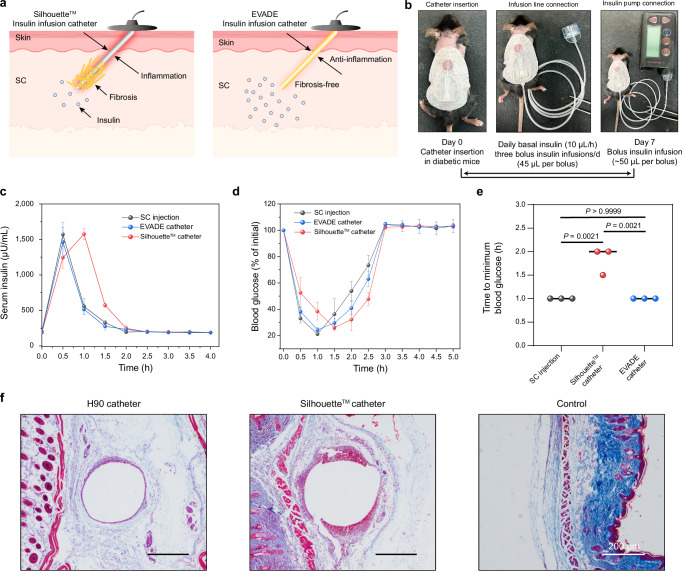
为了验证EVADE弹性体的实际应用价值,研究者开发了由EVADE材料制成的持续皮下胰岛素输注(CSII)导管,并在糖尿病小鼠模型中评估了其在标准泵治疗条件下的性能。实验结果显示,EVADE输注导管在耐久性和性能上显著优于商业导管。通过胰岛素泵进行的推注输注的胰岛素吸收试验表明,与标准皮下(SC)注射相比,通过EVADE导管输送的胰岛素表现出与SC注射一致的药代动力学特征。这表明EVADE材料能够减少局部免疫反应,从而改善植入式生物医学设备的体内性能。
此外,研究者还进行了为期一年的植入研究,并在十二个月后取回弹性体样品进行纤维化评估。实验结果显示,所有H90弹性体样品均显示出清晰的轮廓,并被较薄的纤维囊包围。相比之下,对照的PDMS弹性体在植入后形成了厚厚的胶原层,植入十二个月后完全被覆盖。为了将这些发现扩展到更高级的物种,研究者在健康的食蟹猴皮下植入了H90和PDMS弹性体片。两个月后取出植入物并进行分析,结果显示PDMS样品中存在显著的纤维化反应,而H90的胶原层较薄。这些结果表明EVADE弹性体具有长期抗纤维化作用。
五、研究团队与未来展望
- 研究团队介绍
张鹏研究员是浙江大学高分子科学与工程学系的杰出学者,长期从事生物医用材料的研究工作。他的团队在免疫相容性材料研究方面取得了丰硕的成果。近年来,团队开发了一系列基于两性离子材料的免疫相容水凝胶材料、免疫相容弹性体材料以及基于天然白蛋白的免疫相容表面改性方法。这些研究成果为可植入医疗器械的免疫相容性材料提供了新的思路和方法。
- 未来展望
尽管EVADE弹性体在抗异物反应方面取得了显著成效,但研究者们并没有停止前进的脚步。他们将继续深入研究EVADE弹性体的抗异物反应机制,探索其在更多领域的应用可能性。同时,他们还将致力于开发更多具有优异免疫相容性的生物材料,为可植入医疗器械的发展贡献更多的力量。
六、结论
浙江大学张鹏研究员团队开发出的无需涂层的免疫相容性弹性体——EVADE弹性体,为可植入医疗器械的免疫相容性材料提供了新的选择。该材料具有易于合成、无毒、植入后炎症可忽略不计以及长期抗纤维化作用等优点。通过体内和体外实验验证,研究者们发现EVADE弹性体能够显著降低植入后引发的异物反应,并调节免疫反应。此外,由EVADE材料制成的输注导管在糖尿病小鼠模型中表现出优异的性能。这些发现表明EVADE材料具有广阔的应用前景,有望为生物医学领域带来更多的创新和突破。未来,随着研究的深入和技术的不断发展,相信EVADE弹性体将在更多领域得到广泛应用,为人类健康事业做出更大的贡献。
| 名称 | 货号 | 规格 |
| Mouse IL-17 ELISA Kit | abs520009-96T | 96T |







