高内涵细胞成像与分析技术
铁死亡
铁死亡是一种于2012年由Dixon等人首次阐述的新型细胞程序性死亡模式,近年来相关研究数量急剧增长。该过程受到铁代谢、活性氧(ROS)代谢及脂质代谢的共同调节,并在包括神经系统、心脏、肝脏、胃肠道、肺部、肾脏及胰腺等多个系统疾病的发病机理中扮演着核心角色。
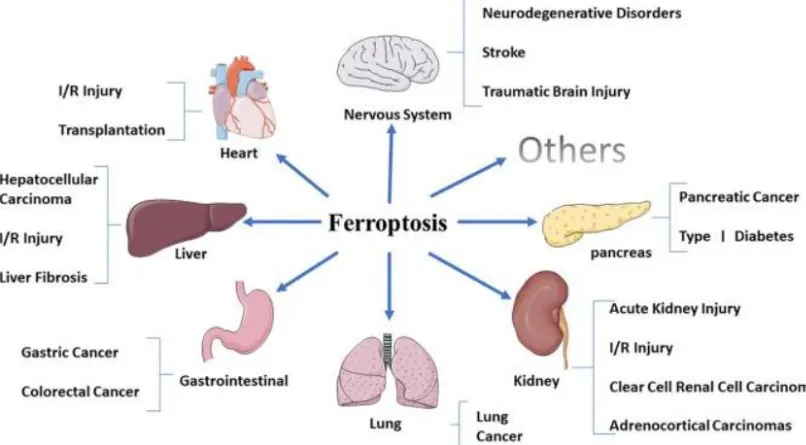
铁死亡的分子机制
铁死亡的分子机制涉及外部与内部两种触发路径。外部路径通常由于细胞膜上的转运蛋白如胱氨酸/谷氨酸转运体(简称XC-系统)受到抑制,或是血清转铁蛋白与乳转铁蛋白的活化而启动。内部路径则是通过阻碍细胞内的抗氧化酶功能,特别是谷胱甘肽过氧化物酶GPX4的活性,进而被激活。这两种路径共同导致了铁死亡的发生。
铁死亡的特征
在形态学方面,铁死亡表现为细胞膜的破裂,线粒体的体积缩小,线粒体嵴的数量减少乃至消失,线粒体膜的密度上升,尽管外膜出现破裂,但细胞核的形态保持正常,并未观察到染色质的凝聚现象。
从生物学特性来看,铁死亡伴随着铁元素与活性氧(ROS)的积累,这会进一步激活丝裂原活化蛋白激酶(MAPK)系统。同时,胱氨酸的摄取量下降,导致细胞内谷胱甘肽(GSH)的耗竭。此外,XC-系统的功能受到抑制,而NADPH氧化酶(NOXs)的活性增强,还会释放花生四烯酸(arachidonic acid; ARA)等生物活性介质。
案例

铁死亡是一种依赖于铁的细胞程序性死亡方式,近年来在众多领域中展现出了关键的作用。最新的研究揭示,细胞对铁死亡的敏感性会随着其状态的不同而有所变化。为了深入探究调控铁死亡敏感性的因子,科研人员采用了全基因组CRISPR/Cas9筛选技术,选取了对铁死亡敏感的肾癌与卵巢癌细胞作为研究对象,结果发现与过氧化物酶体相关的基因出现了显著的富集现象。
随后,研究人员进一步探索了过氧化物酶体对铁死亡敏感性的影响,并发现与合成缩醛磷脂相关的酶类存在显著富集。这些酶类包括脂肪酰基辅酶A还原酶1(FAR1)、编码过氧化物酶体烷基甘油磷酸合酶(AGPS)以及磷酸甘油O-酰基转移酶(GNPAT)等。这些发现为理解铁死亡的敏感性调节机制提供了新的线索。
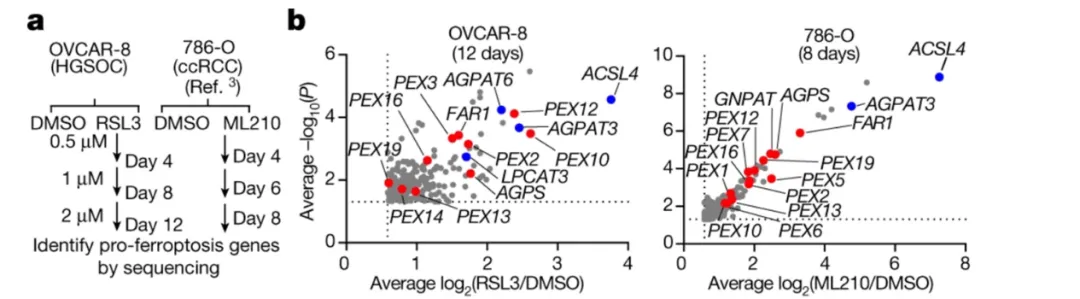
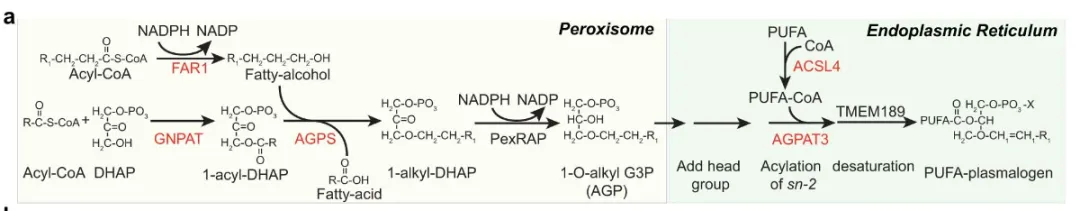
缩醛磷脂是一种独特的磷脂,主要分布于细胞的内膜体系中,其特色在于甘油部分的sn-1位置上含有一个烯醇双键,因此得名。这种磷脂的前体是在过氧化物酶体内合成的,而后续的合成过程则在内质网中进行。鉴于缩醛磷脂含有不饱和双键,它很可能成为脂质过氧化反应以及铁死亡过程中的重要靶标或底物。为了验证这一假设,研究人员采用了纳米颗粒技术,将人工合成的多不饱和磷脂输送到OVCAR-8卵巢癌细胞中,实验结果进一步支持了上述推断。

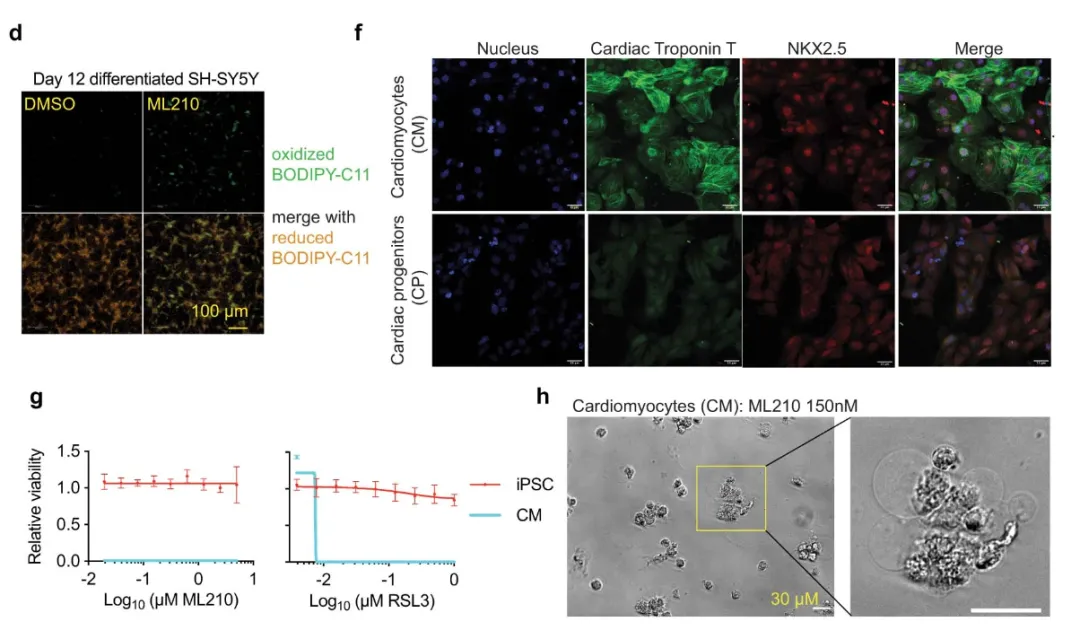
研究人员还发现,在干细胞定向分化为神经细胞(neurons)和心肌细胞(cardiomyocytes)的过程中,缩醛磷脂的含量呈现出特异性上调。这种增加不仅使得细胞对铁死亡的敏感性增强,而且值得注意的是,神经细胞和心肌细胞本身就是机体内缩醛磷脂含量最高的细胞类型,同时它们也是在应激条件下最容易遭受铁死亡威胁的细胞。
为了验证这一点,研究人员采用了高内涵共聚焦成像技术来观察分化的神经细胞和心肌细胞在铁死亡诱导剂(如ML210和RSL3)作用下的变化。如图5所示,分化了12天的神经细胞SH-SY5Y在经过ML210处理后,使用BODIPY-C11(一种能够检测细胞内和细胞膜中活性氧的荧光比值探针)进行成像,结果显示ML210处理组相较于对照组出现了明显的活性氧堆积,从而诱导了铁死亡。同样地,当心肌细胞与多能干细胞分别经过ML210和RSL3处理24小时后,它们的细胞活力显著下降。此外,从明场图像中可以直观地观察到细胞发生了死亡现象。这些结果进一步证实了缩醛磷脂在铁死亡过程中的重要作用。
| 名称 | 货号 | 规格 |
| IVIS Lumina, Series III, 220-240V IVIS Lumina III小动物活体成像主机 | CLS136335 | EA |
| 长时程动态实时活细胞成像分析系统 | Incucyte S3 | 套 |
| 五色成像服务 | mihc-4B5Sphoto-EA | EA |







