表观遗传筛选
近年来,表观遗传药物发现与开发项目吸引了越来越多的关注与资本投入,这主要归因于针对转录和表观遗传相关疾病的新型治疗策略所展现出的巨大潜力。
表观遗传靶点在未来十年被认为是最具前景的一类药物靶点。这类靶点与肿瘤学研究密切相关,并且在代谢、神经、炎症和心血管性疾病的治疗中也显示出一定的潜在影响。高效的表观遗传药物发现与开发需要借助高质量的工具来实现,其中包括重组蛋白、酶类、有效的抗体以及其他表观遗传学的实验途径。

利用重组表观遗传相关酶进行高通量筛选
现今表观遗传研究和药物发现中的一个难关是开发出稳健的适合高通量筛选的酶实验途径。而高效且可靠的筛选,关键在于是否能够连续且有序地获得包括酶和底物在内的高质量的蛋白。
另外,在筛选实验中,蛋白的构象是否正确也十分关键。例如,在筛选鉴定能抑制表观遗传相关酶的小分子药物时,只需要蛋白的催化功能域;而筛选中需要呈现出蛋白高级结构复合物状态时(如干扰蛋白间相互作用的药物),则很可能需要重组蛋白。
组蛋白乙酰转移酶(HATs)和组蛋白去乙酰化酶(HDACs)
组蛋白乙酰转移酶(HATs)和组蛋白去乙酰化酶(HDACs)通过向组蛋白添加或移除乙酰基团,在基因表达调控及其他生物学过程中发挥关键作用。组蛋白的乙酰化通常使染色质结构更加松散,便于DNA相关蛋白(如转录因子)结合,从而与活跃的基因转录密切相关。在正常细胞与癌细胞之间,可以观察到乙酰化模式的显著差异。
近年来,以组蛋白乙酰转移酶和去乙酰化酶作为药物靶点的研究备受关注。由于在多种癌症和其他人类疾病中频繁发现CPB和p300这两种HATs的基因突变,它们已成为研究热点。HDAC1、HDAC2和HDAC3则是HDACs中被广泛研究的几种亚型。
目前,已有几种HDAC抑制剂在临床上得到应用,例如丙戊酸(VPA)用于癫痫、痉挛、躁郁症或偏头痛的治疗,而辛二酰胺(也称为SAHA或伏立诺他)则被用于治疗皮肤T细胞淋巴瘤(CTCL)。
组蛋白甲基转移酶(HMTs)和去甲基化酶(HDMs)
组蛋白甲基转移酶(HMTs)和去甲基化酶(HDMs)通过向组蛋白添加或移除甲基基团,构成了一类关键的表观遗传修饰机制,这亦是当前表观遗传学研究中最为广泛探讨的领域之一。组蛋白的甲基化修饰在生物进程中扮演着举足轻重的角色,涵盖基因表达调控、DNA修复、干细胞的发育与分化以及DNA复制等关键环节。
具体到基因表达调控层面,依据组蛋白残基被修饰位置的差异,组蛋白甲基化既可促使基因转录活跃,亦可使其受到抑制。例如,组蛋白H3第4位赖氨酸(H3K4)的甲基化修饰与基因转录活跃状态紧密相连,而第9位或第27位赖氨酸的甲基化则主要作为基因沉默及异染色质形成的标志性表观遗传信号。
此外,组蛋白甲基化修饰还展现出另一层面的复杂性与规律性。组蛋白赖氨酸残基的甲基化修饰存在甲基基团数量的差异,具体表现为0、1、2或3个甲基化形式(分别记作me0、me1、me2、me3)。不同级别的甲基化状态对表观遗传修饰的功能具有显著影响。
在肿瘤及其他人类疾病中,已发现甲基转移酶与去甲基化酶的异常表达或活性变化,这提示这些表观遗传酶类有望作为相关疾病的药物靶点加以利用。当前,组蛋白甲基转移酶EZH2(作用于H3K27)和DOT1L(作用于H3K79)已成为表观遗传药物研究领域的热点靶点。包括葛兰素史克(GSK)、诺华和Epizyme在内的多家制药公司均启动了针对这两个靶点以及其他甲基转移酶靶点的药物开发项目。
在去甲基化酶研究方面,LSD1则成为主要的药物开发靶点。在多种肿瘤中观察到因基因变异导致的LSD1过表达现象,罗氏、葛兰素史克、新基(Celgene)等公司已开发出针对该酶的小分子抑制剂。
Bromodomain结构域蛋白
Bromodomain结构域蛋白是一类含有约100个氨基酸的蛋白结构域,能够特异性识别并结合乙酰化的赖氨酸残基,其中包括组蛋白中常见的乙酰化修饰位点。这类蛋白在转录调节和染色体重构过程中发挥着不可或缺的作用,并且已证实能够调节数种致癌基因的转录,因此有望成为未来肿瘤治疗的关键靶点之一。
DNA甲基化酶
在多种人类癌症中,已经观测到DNA甲基化水平的变化,这使得作用于DNA甲基转移酶(DNMTs)成为备受关注的治疗靶点。一些抑制DNMTs活性的治疗药剂已被鉴定,如氮杂胞苷,同时还有许多项目正在积极寻找其他有效的药物。此外,一些参与调节DNA甲基化的蛋白,如TET家族,也显示出成为治疗潜在目标的前景。
具体而言,DNMTs在多种癌症中呈现过表达,且与肿瘤的发生及进展呈正相关,这为癌症治疗提供了一个有前景的策略。目前,像氮杂胞苷这样的核苷类DNMT抑制剂已被美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准用于治疗急性髓系白血病(AML)、慢性粒单核细胞白血病(CMML)和骨髓增生异常综合征(MDS)等血液系统恶性肿瘤。此外,非核苷类抑制剂的研究与开发也成为了当前的研究热点,旨在发现更多具有高效性、高选择性和药物特性的DNMT抑制剂。同时,TET家族蛋白作为DNA甲基化过程中的重要调节因子,其在癌症治疗中的潜在价值也正受到越来越多的关注。
表观遗传酶
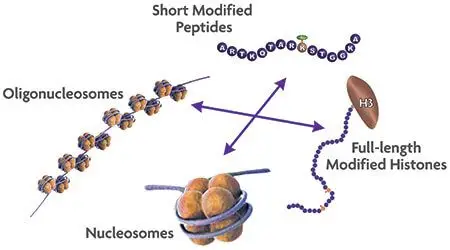
在酶类实验中,确定最适宜的底物与酶本身同等重要。表观遗传酶类在生物体内的天然底物并非游离的组蛋白或短肽段,而是组装到包含DNA的核小体中,并与其他蛋白及RNA共同构成染色质的高级结构。
由于难以在体外精确复制染色质的天然状态,染色质的复杂性和结构的可变性为针对这些酶的药物研发带来了独特的挑战。因此,经修饰的短肽段作为能够高效模拟组蛋白尾巴的替代底物,常被用于高通量筛选。
然而,短肽段无法准确复制生物体内天然底物的状态,有时甚至无法与表观遗传酶类有效相互作用以产生反应。
另一种类型的底物,包括修饰或未修饰的全长组蛋白、组蛋白八聚体、单个核小体和低聚核小体,则表现出更好的与特异性酶结合的能力。因此,在药物研发中,选择合适的底物以确保实验中酶作用的最佳效果是至关重要的决策。
| 名称 | 货号 | 规格 |
| GPCR Agonist-2 | abs824488-10mg | 10mg |
| OXER1/5-oxo-ETE GPCR Ab [PerCP] | NBP2-97990PCP | 0.1ml |
| Human GPCR 2037 Gene Knockout Kit(CRISPR) | abs6115729-1kit | 1kit |
| Human GPCR TGR7 Gene Knockout Kit(CRISPR) | abs6117234-1kit | 1kit |







