Nuclear morphology is shaped by loop-extrusion programs
背景知识
中性粒细胞是人体内含量最丰富的粒细胞类型,约占白细胞总数的40%至70%。这种细胞的细胞核形态独特,呈带状、多分叶状或环状等多种形状,因此又被称为多形核白细胞。中性粒细胞具有穿越血管壁进入组织的能力,其可塑的多形核形状使其能够在组织中狭窄的间隙中灵活迁移【1-3】。尽管越来越多的证据表明,核形状和核可塑性的异常变化与癌症、心脏病和免疫细胞缺陷等多种疾病有关,但调控核形态和核可塑性的分子机制仍然未知。
最新研究进展
近日,美国加州大学的Cornelis Murre课题组在《Nature》杂志上发表了题为“Nuclear morphology is shaped by loop-extrusion programs”的研究论文。该研究揭示了骨髓中性粒细胞祖细胞中的环挤压程序如何诱导产生中性粒细胞特定谱系的染色质结构,从而使染色体能够排列成叶状结构,并通过形成兆环指导该品系细胞特异性基因的表达。

研究意义
这项研究不仅为理解中性粒细胞核形态的形成机制提供了新的视角,还为研究核形态异常与疾病之间的关系奠定了基础。通过深入探索环挤压程序在核形态调控中的作用,未来有望开发出针对相关疾病的新型诊断和治疗方法。
研究背景与模型构建
为了深入探究核形态的决定机制,研究者选用中性粒细胞作为研究模型。他们借助之前构建的髓系中性粒细胞祖细胞的体外培养系统开展研究。在该系统中,当向培养基中添加β-雌二醇时,单核细胞能够实现无限增殖;而一旦移除β-雌二醇,细胞周期便会停滞,且细胞开始分化为多形核中性粒细胞【5,6】。在分化过程中,中性粒细胞中与染色质环挤压相关的基因表达量呈现下降趋势。
关键发现与机制解析
进一步的研究揭示了环挤压装载因子NIPBL缺失所带来的影响。NIPBL的缺失导致细胞周期停滞、细胞死亡率上升,并促使中性粒细胞表面标志物的表达以及建立中性粒细胞特性的转录因子的激活。与此同时,原本呈单核形态的祖细胞迅速形成多形核结构,这一变化与终末分化阶段高分叶中性粒细胞的特征高度一致。这些数据有力地表明,中断中性粒细胞祖细胞中的环挤压过程能够激活中性粒细胞特异性基因程序,并促使细胞形成多形核的组装状态。
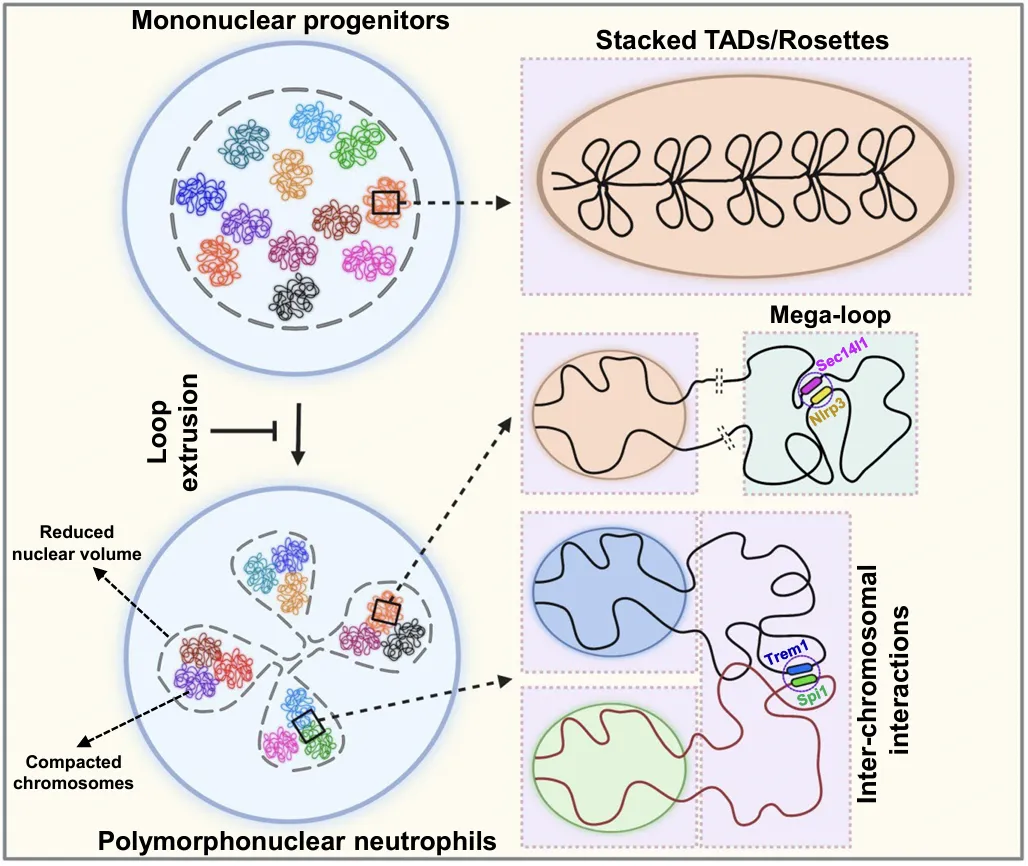
为了进一步探究停止环挤压是否会对染色质组装结构产生影响,研究者运用Hi-C技术展开研究。结果发现,在祖细胞中,NIPBL的缺失导致局部染色体内(<4 Mb)接触频率降低,而远端染色体内(>4 Mb)接触频率升高,拓扑相关结构域(TAD)内的相互作用显著下降。这些染色体的三维结构变化与分化成熟的中性粒细胞中观察到的染色体结构极为相似,并且会促使新的染色质环重新组装,进而激活中性粒细胞特异性基因的表达。在更宏观的维度上,聚集在染色质B区的巨大兆环(Mega-loop)平均跨越长度长于染色质A区的兆环长度。NIPBL缺失后,兆环内部TAD的接触频率显著下降,这些变化与mRNA和染色质开放水平的变化密切相关。具体而言,受影响的基因富集了炎症特异性基因。当环挤压停止时,中性粒细胞祖细胞中形成兆环,将位置较远的增强子和启动子配对到共同的转录中心,从而驱动中性粒细胞特异性基因的表达。此外,NIPBL的缺失也是引发多形核变化的关键调控步骤。
体内验证与结论
最终,研究者将体外研究的发现成功地在体内进行了验证。他们通过电穿孔技术将NIPBL靶向的CRISPR RNA(crRNA)转导至骨髓中性粒细胞祖细胞中,实现NIPBL的缺失。经过这一操作,原代中性粒细胞祖细胞中,前体细胞、髓细胞和间变性髓细胞数量减少,而各类中性粒细胞数量显著增加,中性粒细胞表面标志物含量也大幅提升。此外,单细胞RNA测序(scRNA-seq)数据进一步证实了这一发现,NIPBL缺失显著富集了分化的中性粒细胞。
| 名称 | 货号 | 规格 |
| Rabbit anti-SMC1 Antibody, Affinity Purified | A300-055A | 100 µl (1000 µg/ml) |
| Anti-Rad21 antibody | ab992-50ug | 50ug |
| RT? Profiler PCR Array - Plate C 12 Arrays | 330231-PlateC12Arrays | 12plates |
| Anti-SMC3 antibody | ab9263-50ug | 50ug |






