外泌体DNA提取
外泌体作为细胞衍生的纳米级膜性囊泡,其内容物囊括了细胞质中几乎所有类别的生物活性分子谱系,包括但不限于功能蛋白组、非编码RNA分子库及代谢小分子网络。这些内含物通过精密调控的分子分选机制实现动态组装,在供体-受体细胞间构建起复杂的信号转导网络,已成为细胞间通讯研究领域的核心载体。值得注意的是,尽管真核细胞遵循严格的基因组守恒机制以维持遗传信息稳定性,但外泌体是否包含核DNA组分始终是该领域长期存在的科学悖论。传统观点认为,细胞核基因组的完整性是维持基本生命活动的基础,而胞外囊泡介导的DNA分泌可能引发遗传信息泄露风险,这种表观矛盾使得外泌体DNA载运现象的分子机制与生物学意义至今尚未得到系统性阐释,成为制约胞外囊泡生物学功能解析的关键瓶颈问题。
角度一
外泌体DNA的来源?
当前对于外泌体DNA的起源机制尚未形成完整认知,学界推测其可能通过两条独立途径实现生物学发生[1]:其一为基因组DNA损伤修复过程中产生的单链或双链DNA片段,经由细胞内膜系统分选机制实现囊泡化封装,形成具有膜性屏障保护的腔内核酸组分;其二为邻近细胞发生程序性死亡时释放的染色质片段,通过静电相互作用非共价结合于细胞分泌外泌体的脂质双层表面,构成膜相关核酸复合体。值得注意的是,上述两种假说仅能部分解释现有实验现象,外泌体DNA是否还存在其他未被阐明的生物合成路径,仍有待多组学技术的深入解析。
 外泌体DNA生成
外泌体DNA生成
角度二
基于外泌体DNA的生物发生机制推演,其是否必然呈现膜内包裹与膜外吸附的双重存在形式?
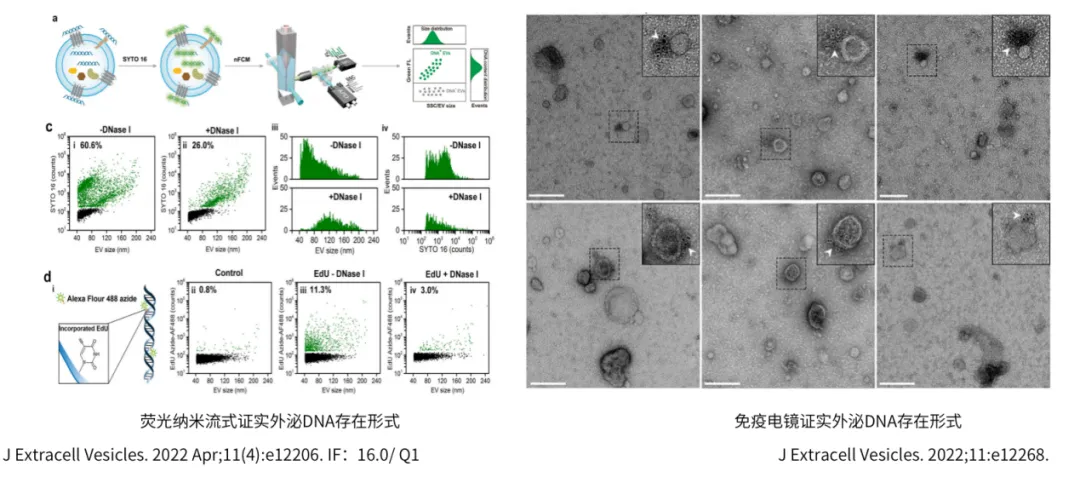
2022年发表于《Journal of Extracellular Vesicles》的两项独立研究通过多模态技术手段对该命题进行了系统性验证:研究团队采用SYTO 16核酸荧光探针特异性标记策略,结合纳米流式细胞术对单颗粒外泌体进行高维参数分析,实验结果显示外泌体相关DNA既可检测到膜性结构包裹的腔内信号,亦存在显著富集于脂质双层外表面的膜关联信号,且后者占据总检测信号量的78.6±5.2%[2];另一项研究则运用免疫胶体金标记结合冷冻透射电镜三维重构技术,在亚纳米级分辨率下直接观测到外泌体表面附着的DNA-蛋白复合体结构[3]。上述技术体系不仅从形态学层面印证了外泌体DNA的双重存在模式,更通过交叉验证确立了膜外吸附形式的主导地位,为解析此类核酸组分的生物学功能奠定了方法学基础。
角度三
鉴于外泌体内容物固有的微量特征及其组分浓度跨度跨越多个数量级,外泌体DNA是否呈现与RNA组分相似的低丰度、片段化特性?
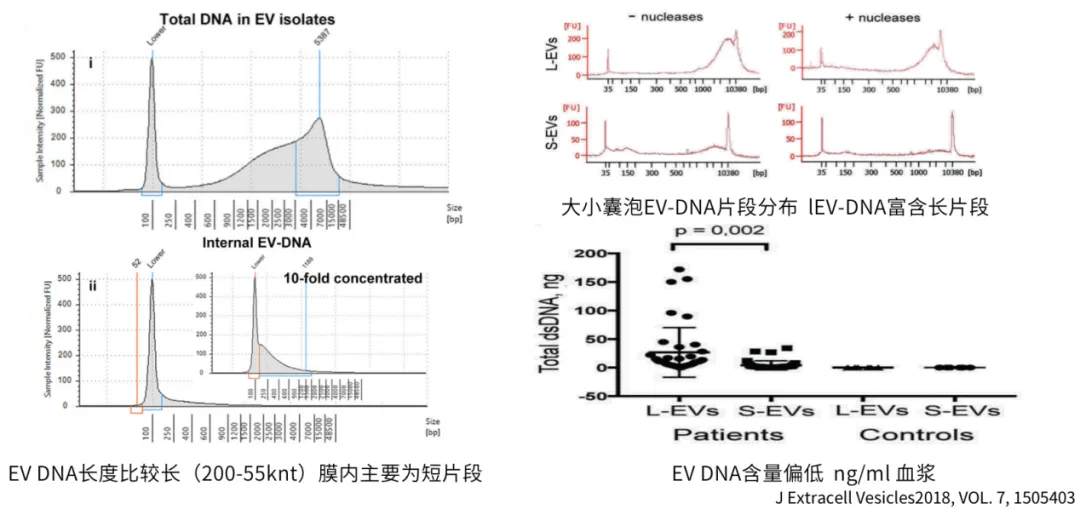
现有研究证实,外泌体DNA具有典型的高度片段化特征,其片段长度呈现200 bp至55 kbp的宽幅分布谱系,且主峰分布呈现显著的组织特异性——健康个体血浆来源外泌体DNA的主峰集中于180-220 bp区间,而肿瘤患者样本则检测到3-5 kbp的异常扩增峰型[4]。值得关注的是,循环系统中外泌体DNA的绝对含量可低至0.15-0.35 ng/mL血浆,这种极低丰度特征对检测技术的灵敏度提出严峻挑战。从分子特征谱系分析,外泌体DNA与循环游离DNA(cfDNA)在片段化模式、核酸修饰图谱等维度均表现出惊人的表型趋同性,这种分子层面的相似性不仅暗示两者可能共享部分生物发生通路,更为借鉴cfDNA领域成熟的液态活检技术体系进行外泌体DNA功能解析提供了重要的方法学借鉴。
自二十世纪八十年代初外泌体生物学功能研究肇始,学界即围绕其是否携带遗传物质展开激烈争论。尽管早期研究通过密度梯度离心联合核酸酶保护实验初步揭示外泌体囊泡内可能存在核酸组分,但受限于检测灵敏度与特异性,其存在性争议持续数十年之久。直至单颗粒水平检测技术突破,研究者运用纳米流式检测技术结合DNA特异性荧光探针,首次在单外泌体分辨率下直接观测到膜结构包裹的核酸信号;同期发展的超分辨显微成像技术更在三维空间解析层面,清晰呈现外泌体表面附着的DNA-蛋白复合体拓扑结构。这些技术革新不仅从方法学层面终结了长期存在的认知分歧,更激发了科研界对胞外囊泡遗传物质功能的探索热情。现有证据表明,外泌体DNA既可作为肿瘤早筛、器官移植排异监测等临床场景的液体活检标志物,亦能通过水平转移至受体细胞介导表观遗传调控,参与肿瘤耐药、免疫逃逸等病理过程。这种兼具生物标志物属性与功能调控潜能的双重特性,使外泌体DNA研究迅速崛起为细胞外囊泡生物学与精准医学交叉领域的前沿热点,其转化医学应用潜力亟待通过多中心队列研究与技术标准体系构建予以深入挖掘。
参考文献:
[1]Ghanam J, Chetty VK, Barthel L, Reinhardt D, Hoyer PF, Thakur BK. DNA in extracellular vesicles: from evolution to its current application in health and disease. Cell Biosci. 2022 Mar 28;12(1):37.
[2]Liu H, Tian Y, Xue C, Niu Q, Chen C, Yan X. Analysis of extracellular vesicle DNA at the single-vesicle level by nano-flow cytometry. J Extracell Vesicles. 2022 Apr;11(4):e12206.
[3]Sedej I, Štalekar M, Tušek Žnidarič M, Goričar K, Kojc N, Kogovšek P, Dolžan V, Arnol M, Lenassi M. Extracellular vesicle-bound DNA in urine is indicative of kidney allograft injury. J Extracell Vesicles. 2022 Sep;11(9):e12268.
[4]Vagner T, Spinelli C, Minciacchi VR, Balaj L, Zandian M, Conley A, Zijlstra A, Freeman MR, Demichelis F, De S, Posadas EM, Tanaka H, Di Vizio D. Large extracellular vesicles carry most of the tumour DNA circulating in prostate cancer patient plasma. J Extracell Vesicles. 2018 Aug 7;7(1):1505403.
| 名称 | 货号 | 规格 |
| 外泌体DNA提取试剂盒 | abs60364-50T | 50T |
| 外泌体DNA提取试剂盒 | abs60364-100T | 100T |
| 人宫颈癌类器官培养基 | abs9639-500ml | 500ml |
| 人宫颈癌Hela细胞外泌体 | abs90123-1mL | 1mL |







