Mendelian randomisation and experimental medicine approaches to interleukin-6 as a drug target in pulmonary arterial hypertension
一、引言
肺动脉高压(PAH)是一种罕见且常致命的疾病,其特征是小肺动脉的显著重塑,导致肺血管阻力(PVR)增加和右心衰竭。尽管存在多种治疗方法,但死亡率仍然较高,迫切需要识别新的治疗方法。白细胞介素-6(IL-6)信号通路在 PAH 中具有重要作用,然而托珠单抗(tocilizumab)在一项 2 期临床试验中未显示出显著效果。本文将深入解析 Mark Toshner 等人发表在《European Respiratory Journal》上的研究,探讨 IL-6 作为 PAH 治疗靶点的潜力。
二、研究背景
PAH 的发病机制涉及炎症和免疫失调。IL-6 水平在 PAH 患者的外周血和肺部均一致升高,且 IL-6 是预后的独立标志物。动物模型中,IL-6 的过表达可促进肺动脉高压的发生,而 IL-6 缺陷小鼠则受到保护。托珠单抗是一种 IL-6 受体(IL-6R)拮抗剂,在类风湿性关节炎(RA)等疾病中已证明安全有效。基于此,研究团队开展了托珠单抗在 PAH 治疗中的 2 期临床试验,并通过孟德尔随机化研究进一步探讨 IL-6R 在 PAH 中的因果关系。
三、研究方法
(一)临床试验设计
研究招募了 29 名 PAH 患者,包括特发性或遗传性 PAH 以及结缔组织病相关 PAH(CTD-PAH)患者。患者接受每月一次静脉注射托珠单抗(8 mg·kg⁻¹),共 6 个月。主要终点为安全性(通过不良事件发生率和严重程度评估)和 PVR 变化(通过右心导管测量)。
(二)孟德尔随机化研究
研究团队对 11744 名具有欧洲血统的个体(包括 2085 名特发性/遗传性 PAH 患者)进行分析,研究 IL-6R 变异(rs7529229)与 PAH 风险之间的关系。该变异与循环 IL-6R 水平相关。
四、实验结果
(一)临床试验结果
-
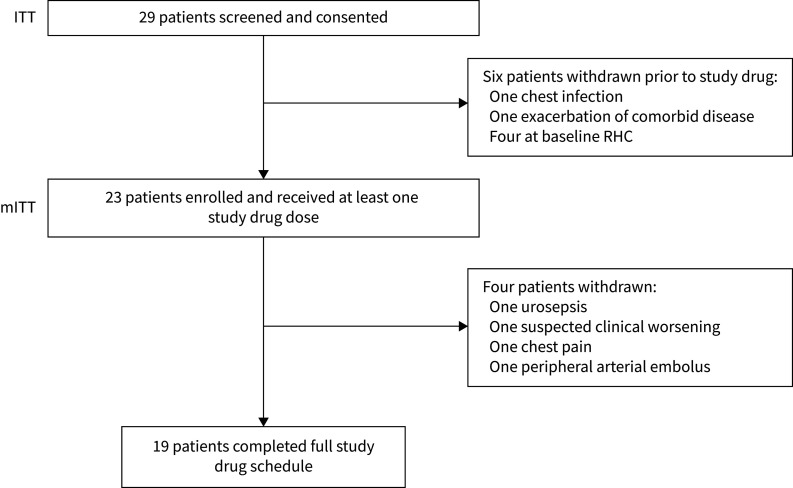
患者招募与治疗情况:共招募 29 名患者,其中 23 名接受了至少一剂托珠单抗。四名患者因严重不良事件停药,但无死亡病例。
-
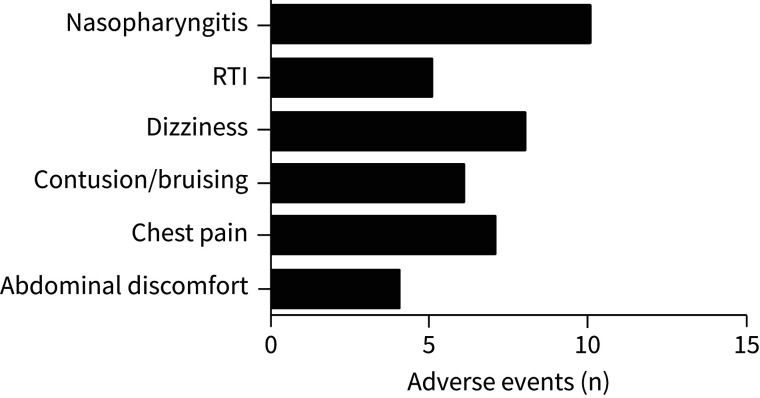
安全性结果:托珠单抗的安全性与已知的药物特性一致,最常见的不良事件为鼻咽炎。不良事件大多为轻度(80.0%)或中度(16.6%),严重不良事件仅占 3.4%。
-
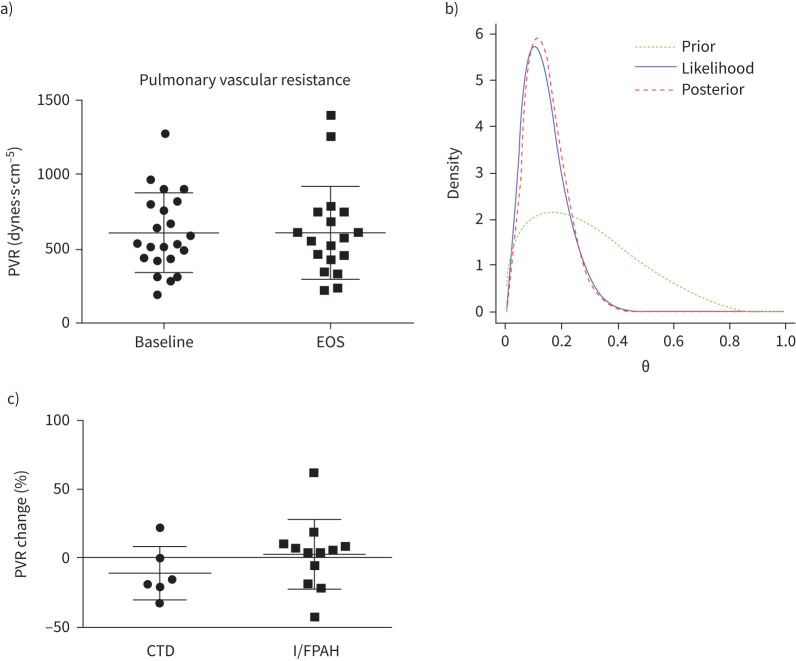
PVR 变化:意向治疗(ITT)和修改意向治疗(mITT)分析均显示,托珠单抗治疗 6 个月后 PVR 未发生显著变化。在 CTD-PAH 患者中,六名接受治疗的患者中有四名 PVR 降低超过 15%,而特发性或遗传性 PAH 患者中 13 名有三名 PVR 降低超过 15%。
-
其他终点:6 分钟步行距离(6MWT)平均增加 19.1±60.8 米,NT-proBNP 中位数增加 22.5 pg·mL⁻¹(IQR 275 pg·mL⁻¹),CAMPHOR 评分中位数降低 2(IQR 10)。WHO 功能分级在六名患者中改善,在四名患者中恶化。
(二)孟德尔随机化结果
-
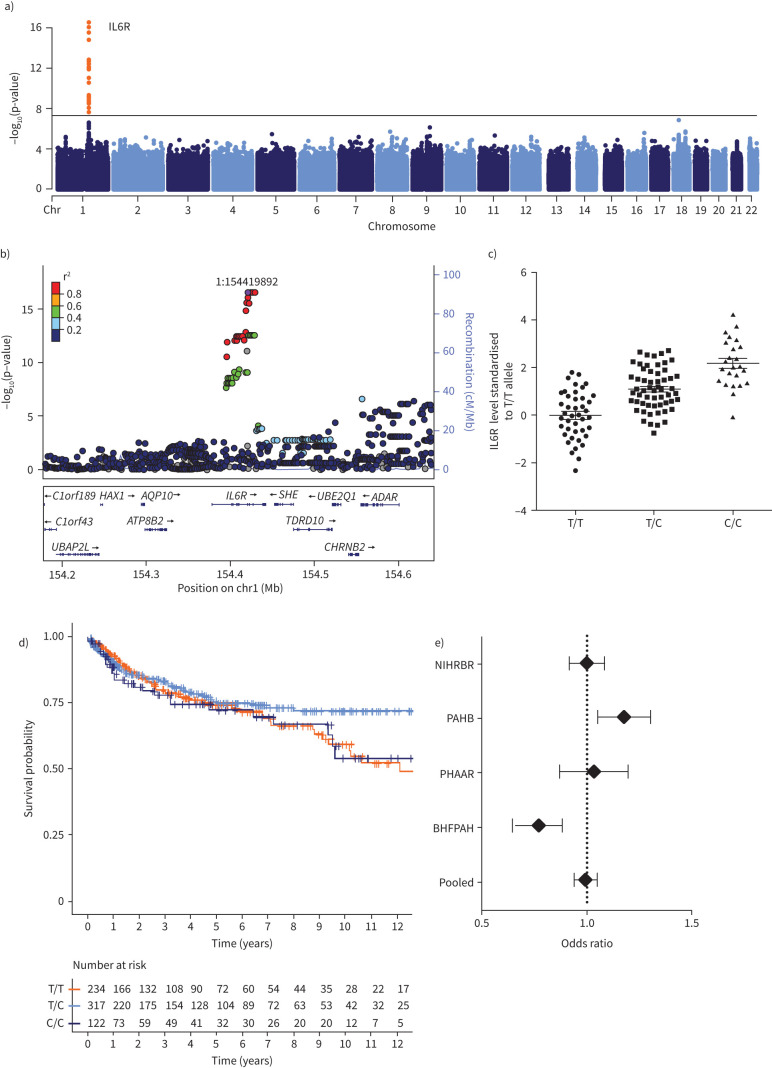
IL-6R 变异与循环 IL-6R 水平:rs7529229 的每个次要等位基因 “C” 与循环 IL-6R 水平增加相关(效应估计值 0.27±0.03,P=2.69×10⁻¹⁶)。
-
IL-6R 变异与 PAH 风险:在 2085 名特发性或遗传性 PAH 患者和 9659 名对照的孟德尔随机化分析中,rs7529229 与 PAH 风险无显著关联(OR 0.99,95% CI 0.9–1.09,P=0.88)。此外,IL-6R SNP rs7529229 的基因型与 NIHRBR 研究队列中的全因死亡率也无关联。
五、研究结论
研究发现托珠单抗在特发性或遗传性 PAH 患者中未显示出对 PVR 或其他探索性终点的一致治疗效果。孟德尔随机化研究结果也未支持 IL-6R 在 PAH 中的因果关系。尽管如此,在 CTD-PAH 患者亚组中观察到潜在的改善,这值得进一步研究。
六、研究意义与启示
该研究首次结合遗传数据和早期临床试验测试 IL-6 作为 PAH 治疗靶点的潜力,为未来药物开发提供了新的思路。尽管在整体 PAH 患者群体中未观察到显著效果,但在 CTD-PAH 患者中的初步积极信号提示未来研究可聚焦于特定亚组患者,并考虑疾病早期的患者分层和分型。
七、研究局限性
-
样本量有限:研究样本量较小,可能导致统计功效不足,难以检测到较小的治疗效果。
-
开放标签设计:缺乏安慰剂对照,可能影响对治疗效果的准确评估。
-
观察期限较短:6 个月的观察期可能不足以评估免疫调节治疗对 PVR 的潜在长期影响。
八、未来研究方向
未来的研究可进一步扩大样本量,延长观察期限,并在 CTD-PAH 患者中开展针对性的随机对照试验。此外,结合遗传数据和多组学技术,探索 IL-6 信号通路在 PAH 不同亚型中的作用机制,为精准治疗提供依据。
参考文献
Toshner M, Church C, Harbaum L, et al. Mendelian randomisation and experimental medicine approaches to interleukin-6 as a drug target in pulmonary arterial hypertension. Eur Respir J 2022; 59: 2002463 [DOI: 10.1183/13993003.02463-2020].
图表和数据
图 1:研究流程图
展示了研究筛选和入组过程,包括意向治疗(ITT)和修改意向治疗(mITT)人群的构成。
图 2:常见不良事件
展示了按照 MedDRA 编码的常见不良事件的绝对数量,鼻咽炎是最常见的不良事件。
图 3:PVR 变化
(A)所有患者基线和研究结束时的 PVR 绝对值;(B)基于 mITT 的贝叶斯分析;(C)按疾病分组的 mITT 百分比变化。结果显示托珠单抗治疗未显著改变 PVR。
图 4:IL-6R 孟德尔随机化
(A)全基因组关联研究中的蛋白数量性状定位(pQTL);(B)pQTL 的 locus zoom 图;(C)不同基因型下循环 IL-6R 水平;(D)NIHRBR 研究队列的生存分析;(E)国际研究的森林图荟萃分析。孟德尔随机化分析表明 IL-6R 变异与 PAH 风险无显著关联。
表 1:基线人口统计学特征
| 人口统计学变量 | 合并人群 |
|---|---|
| 性别 M/F (n) | 10/19 |
| 年龄(岁,均值±SD) | 54.9±11.4 |
| IPAH/FPAH/CTD (n) | 15/4/10 |
| PVR dyn·s·cm⁻⁵(均值±SD) | 612.30±317.63 |
| mPAP mmHg(均值±SD) | 43.57±11.07 |
| NT-proBNP pg·mL⁻¹(中位数(IQR)) | 329.50 (549) |
| 心输出量 L·min⁻¹(中位数(IQR)) | 5.14 (2.18) |
| PAH 药物治疗(%) | |
| 安立生坦/波生坦/马西滕坦 | 17.2/6.9/3.4 |
| 西地那非/他达拉非/利奥西呱 | 58.6/13.8/11.1 |
| 6 分钟步行距离(均值±SD) | 425.9±112.1 |
| WHO II/III 级(%) | 48.3/51.7 |
表 2:次要终点
| 次要终点 | 合并人群 |
|---|---|
| 6MWT Δ 米(均值±SD) | 19.1±60.8 |
| NT-proBNP Δ pg·mL⁻¹(中位数(IQR)) | 22.5 (275) |
| 博格评分 Δ(均值±SD) | 0.05±0.05 |
| CAMPHOR Δ(中位数(IQR)) | -2 (10) |
| WHO 功能分级:未改变/改善/恶化(n) | 17/4/2 |
注:IPAH:特发性肺动脉高压;FPAH:家族性肺动脉高压;CTD:结缔组织病;PVR:肺血管阻力;mPAP:平均肺动脉压;NT-proBNP:N 末端 B 型利钠肽前体;IQR:四分位距;6MWT:6 分钟步行测试;WHO:世界卫生组织;IL-6:白细胞介素-6;CRP:C 反应蛋白。
| 名称 | 货号 | 规格 |
| V-PLEX Proinflammatory Panel1 (human) Kit (25 Plate) | K15049D-4 | 25Plate |
| V-PLEX Proinflammatory Panel1 (human) Kit (5 Plate) | K15049D-2 | 5Plate |
| V-PLEX Proinflammatory Panel1 (human) Kit (1 Plate) | K15049D-1 | 1Plate |