SARS-CoV-2 mRNA vaccine induces robust specific and cross-reactive IgG and unequal neutralizing antibodies in naive and previously infected people
摘要
本研究通过对168名健康医护工作者(包括148名未感染者和20名既往感染者)进行mRNA疫苗接种前后多时间点血清学分析,揭示了BNT162b2/mRNA-1273疫苗诱导的抗体应答特征。研究发现,尽管两组人群在完成全程接种后均产生高水平的刺突蛋白特异性IgG,但中和抗体反应存在显著异质性:40%未感染者在完成接种后仍检测不到有效中和抗体,而既往感染者中仍有20%未产生充分中和活性。此外,疫苗对Delta变异株的中和效率较参考毒株下降20-30%,且季节性冠状病毒交叉抗体在既往感染者中呈现独特动力学特征。
一、研究背景与方法学设计
1.1 研究队列与样本采集
研究纳入237名医护工作者,最终168名完成mRNA疫苗接种(161名BNT162b2,7名mRNA-1273)。通过RT-PCR和血清学检测(核衣壳蛋白抗体及RBD抗体)确定感染状态(图S1):
- 既往感染组(n=20):有症状轻症感染史
- 未感染组(n=148)
纵向采集三个时间点血清: - 接种前(基线,n=136)
- 首剂后6-28天(中位21天,n=149)
- 第二剂后20-66天(中位54天,n=139)
1.2 检测方法
- 结合抗体:ELISA检测全长刺突蛋白、RBD、NTD的IgG/IgM/IgA
- 中和抗体:
- 活病毒中和试验(WIV04参考株,BSL-3实验室)
- 假病毒ACE2结合抑制试验(覆盖7种变异株)
- 交叉反应抗体:ELISA检测4种季节性冠状病毒(HCoV-OC43/HKU1/NL63/229E)刺突蛋白抗体
二、核心研究结果
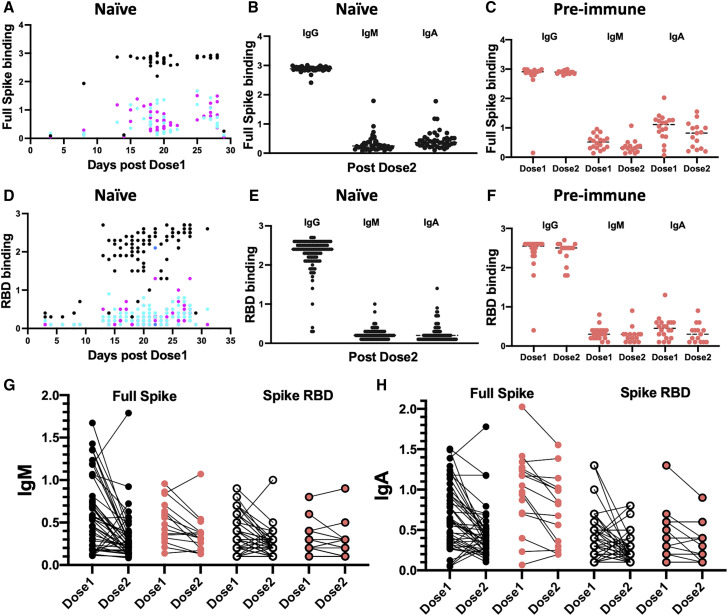
2.1 抗体同种型动态特征(图1)
2.1.1 IgG主导应答
- 首剂后:95%未感染者在接种8天后出现RBD/全长刺突蛋白IgG血清转化
- 第二剂后:两组IgG水平无显著差异(p>0.05)
2.1.2 IgM与IgA应答差异
| 抗体类型 | 未感染组 | 既往感染组 |
|---|---|---|
| IgM | 首剂后升高,二剂后下降 | 整体低于未感染组 |
| IgA | 首剂后升高,二剂后下降 | 首剂后与未感染组相当,二剂后无变化 |
图1G-H:未感染组IgM/IgA在第二剂后显著下降(p<0.001),而既往感染组IgA维持稳定。
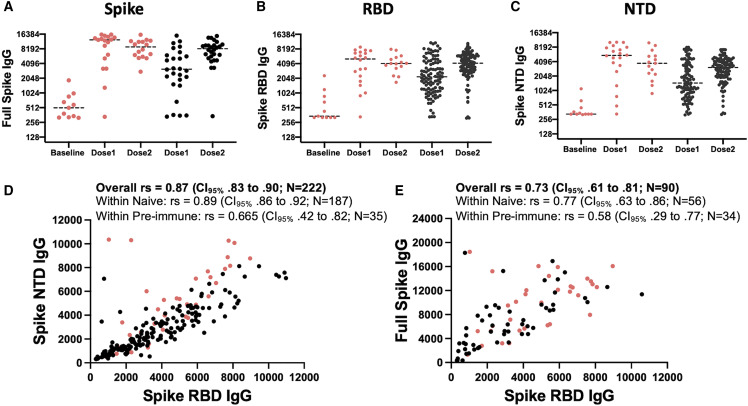
2.2 刺突蛋白结合抗体强度(图2)
- 首剂后:既往感染组RBD/全长刺突蛋白IgG水平显著高于未感染组(AUC差值>2倍)
- 第二剂后:两组IgG水平趋近(图2B-C)
- 相关性分析:RBD抗体与NTD/全长刺突抗体高度相关(rs=0.87, 95%CI 0.83-0.90)
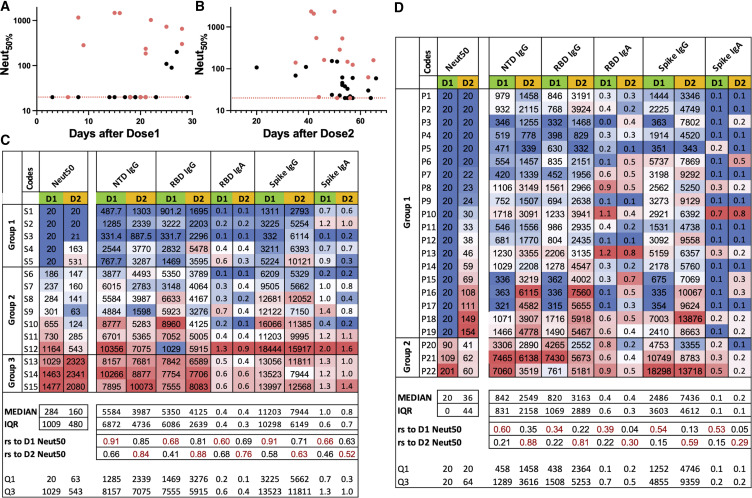
2.3 中和抗体应答异质性(图3)
2.3.1 组间差异
- 第二剂后中和抗体阳性率:
- 未感染组:60%(22/37)
- 既往感染组:80%(16/20)
- 中和效价(Neut50):
- 未感染组中位值:240
- 既往感染组中位值:960
2.3.2 中和抗体动态分组
基于首剂与二剂后变化分为三组:
| 分组 | 特征 | 占比(未感染组) | 占比(既往感染组) |
|---|---|---|---|
| 组1 | 首剂无中和活性,二剂后仍无/弱 | 40% | 20% |
| 组2 | 首剂高效价,二剂后下降 | 30% | 35% |
| 组3 | 首剂低效价,二剂后显著升高 | 30% | 45% |
图3C-D:组2个体虽结合抗体水平高(RBD AUC>0.8),但中和活性在二剂后下降,提示表位质量差异。
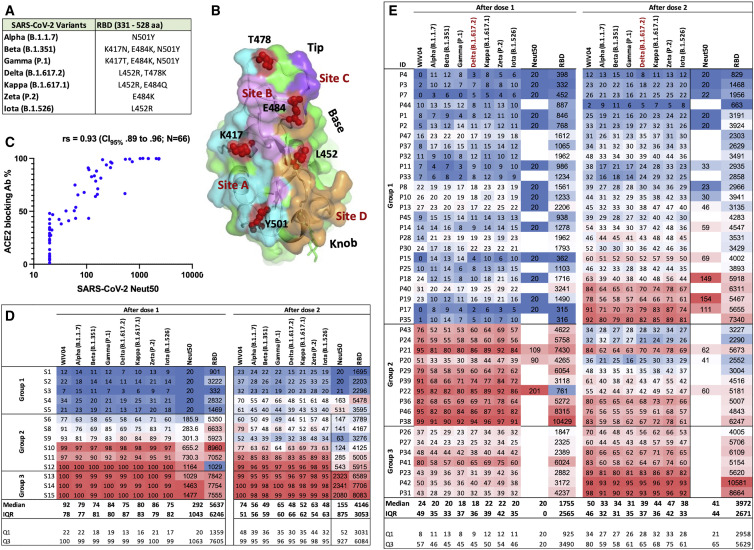
2.4 变异株中和逃逸特征(图4)
2.4.1 ACE2结合抑制率比较
| 毒株 | 未感染组抑制率(%) | 既往感染组抑制率(%) |
|---|---|---|
| 参考株WIV04 | 85.2 ± 6.3 | 92.1 ± 4.8 |
| Delta | 64.5 ± 8.7* | 72.3 ± 7.2* |
| Alpha | 71.2 ± 7.5* | 79.6 ± 6.1* |
| Beta | 68.9 ± 9.1* | 75.4 ± 8.3* |
*注:*表示较参考株下降显著(p<0.01)
2.4.2 逃逸机制解析
- Delta变异株在RBD关键表位累积突变(L452R, T478K)
- 主要中和表位(Site A和Site D)构象改变(图4B)
- 50%以上高效中和抗体(IGHV3-53/3-66家族)对Delta株结合力下降>60%
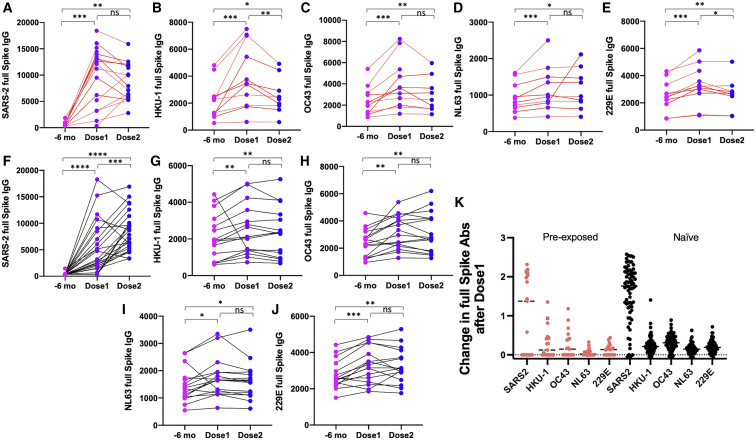
2.5 季节性冠状病毒交叉抗体(图5)
2.5.1 动力学差异
| 抗体类型 | 未感染组 | 既往感染组 |
|---|---|---|
| β-HCoV交叉抗体(OC43/HKU1) | 二剂后持续升高 | 首剂后达峰,二剂后下降 |
| α-HCoV交叉抗体(NL63/229E) | 二剂后轻度升高 | 无显著变化 |
2.5.2 临床意义
- 交叉抗体与SARS-CoV-2抗体水平正相关(rs=0.62-0.71)
- 但未发现与疾病严重程度或保护作用的直接关联
三、讨论与临床启示
3.1 中和抗体异质性的机制探讨
研究发现40%未感染者在完成接种后未检测到中和抗体,可能涉及以下机制:
- 表位聚焦差异:自然感染诱导更广谱表位应答(Greaney et al., 2021b)
- 年龄因素:中和抗体水平与年龄负相关(图S4,rs=-0.43)
- 记忆B细胞库差异:既往感染者存在交叉反应性记忆B细胞(Sokal et al., 2021)
3.2 对疫苗接种策略的启示
- 既往感染者仍需两剂疫苗:33%首剂后无中和活性,其中40%在第二剂后产生中和抗体
- 剂量间隔优化:组2个体(30%)中和效价在3-4周间隔后下降,支持延长间隔至6-12周(Payne et al., 2021)
- 加强针必要性:Delta株中和效率下降及抗体衰减(>6个月)提示需变异株适应性疫苗
3.3 诊断与监测意义
- 核衣壳蛋白抗体:随时间显著衰减(图S1E),不适合长期感染史追溯
- 非刺突蛋白靶点:ORF8/ORF3b抗体可作为疫苗接种者自然感染标志物
四、研究局限性与未来方向
4.1 局限性
- 未包含细胞免疫应答分析
- 未覆盖极端年龄/免疫抑制人群
- 样本采集时间点存在波动(首剂后3-29天,二剂后20-66天)
4.2 未解问题
- 中和抗体阴性者是否通过Fc效应或T细胞获得保护?
- 交叉抗体是否影响后续变异株易感性?
- 黏膜IgA(特别是分泌型IgA2)在呼吸道保护中的作用?
五、结论
本研究揭示mRNA疫苗在未感染与既往感染人群中诱导不均衡的中和抗体应答:
- 结合抗体:两组均产生高水平的刺突蛋白特异性IgG
- 中和抗体:40%未感染者全程接种后无有效中和活性,且对Delta株效率下降20-30%
- 交叉反应:季节性冠状病毒抗体在既往感染者中呈独特动力学
这些发现支持个体化疫苗接种策略及针对变异株的疫苗优化需求。
| 名称 | 货号 | 规格 |
| Peroxidase-conjugated AffiniPure™ Goat Anti-Human IgM, Fc5µ Fragment Specific | 109-035-043 | 2ml |
| V-PLEX SARS-CoV-2 Panel 13 (ACE2) Kit (5 PL) | K15466U-2 | EA |
| V-PLEX SARS-CoV-2 Panel 13 (ACE2) Kit (25 PL) | K15466U-4 | 1EA |








