GLP-1 receptor signaling increases PCSK1 and β cell features in human α cells
引言
2型糖尿病(T2DM)的主要特征是胰岛功能障碍,具体表现为β细胞胰岛素分泌不足和α细胞胰高血糖素分泌过多。胰高血糖素样肽-1(GLP-1)是一种由肠道L细胞和胰岛α细胞产生的肠促胰岛素激素,能够增强葡萄糖刺激的胰岛素分泌(GSIS)。GLP-1通过其受体GLP-1R发挥作用,激活腺苷酸环化酶,增加细胞内cAMP水平,从而增强胰岛素分泌。除了在L细胞中产生外,α细胞在特定条件下也可以表达前 prohormone convertase 1/3(PC1/3,基因名为PCSK1),并产生GLP-1。然而,α细胞中PCSK1表达的调控机制尚不清楚。
研究方法
研究团队通过一系列体内外实验,探讨了GLP-1R激动剂利拉鲁肽(liraglutide)对α细胞GLP-1和PCSK1表达的影响。实验设计包括:
动物实验:使用 tamoxifen 诱导的β细胞特异性GLP-1R敲除(KO)小鼠模型,评估利拉鲁肽对α细胞GLP-1生产和PCSK1表达的影响。
单细胞RNA测序(scRNA-Seq):应用DART-Seq技术,对人类胰岛细胞进行单细胞转录组分析,以高灵敏度检测低丰度转录本。
免疫组化(IHC):对小鼠和人类胰岛样本进行免疫染色,以验证GLP-1和PCSK1的表达变化。
活性GLP-1测量:使用电化学发光免疫分析法测量人类胰岛样本中活性GLP-1的含量。
研究结果
β细胞GLP-1R信号增强α细胞PCSK1和GLP-1表达
小鼠模型实验:
 图一
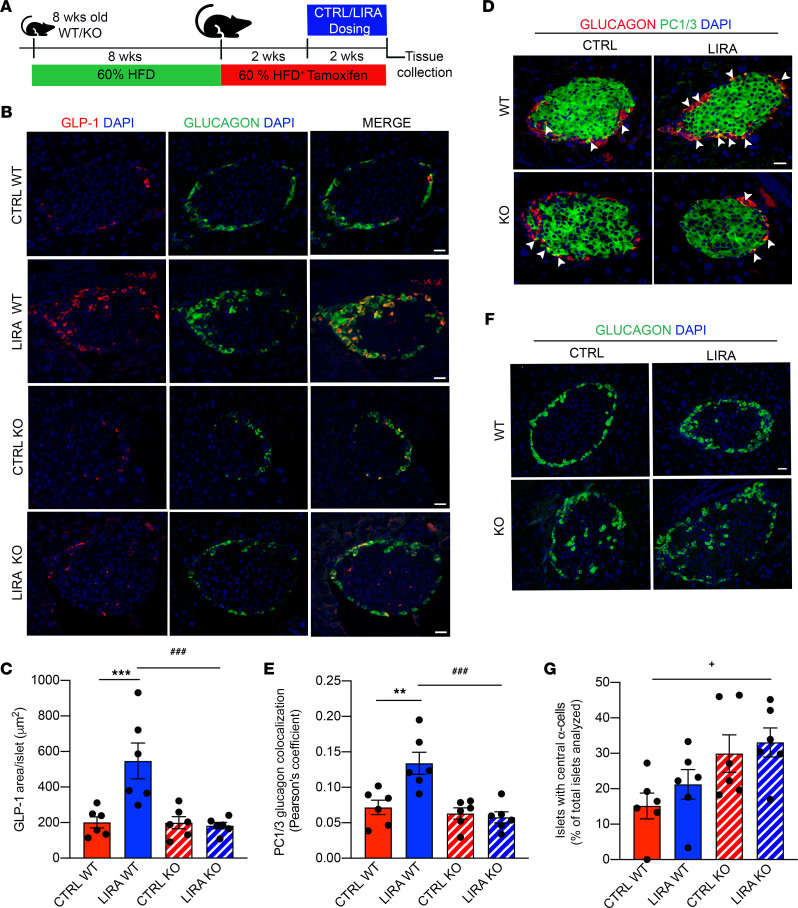
图一
研究发现,利拉鲁肽处理能够显著增加野生型(WT)小鼠胰岛中GLP-1的染色强度,而在GLP-1R敲除(KO)小鼠中则无此效果(图1B和1C)。
免疫共染色显示,利拉鲁肽处理显著增加了WT小鼠α细胞中PC1/3与胰高血糖素的共定位,而在KO小鼠中未观察到这一现象(图1D和1E)。
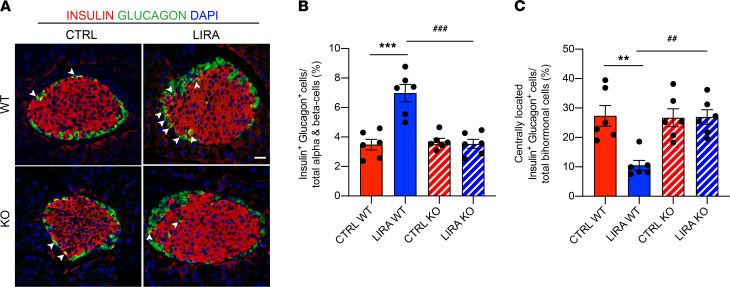
进一步分析发现,β细胞GLP-1R的缺失导致胰岛中中央定位的α细胞数量增加,表明β细胞GLP-1R信号对维持正常的胰岛形态具有重要作用。
DART-Seq技术验证:
 图二
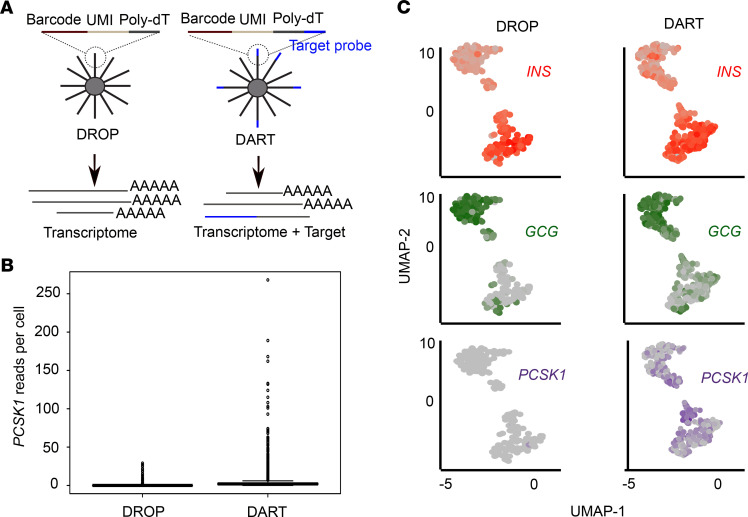
图二
DART-Seq技术改进了对低丰度转录本的检测灵敏度,特别是在人类胰岛α细胞中检测到PCSK1表达(图2A至2C)。
通过DART-Seq分析,研究发现利拉鲁肽处理显著增加了人类胰岛α细胞亚群中PCSK1的表达,并伴随β细胞相关基因(如INS、IAPP和MAFA)的表达增加。
单细胞转录组分析:
单细胞转录组分析揭示了α细胞和β细胞的显著异质性,不同亚群的细胞在成熟度和功能相关基因表达上存在差异。
 图三
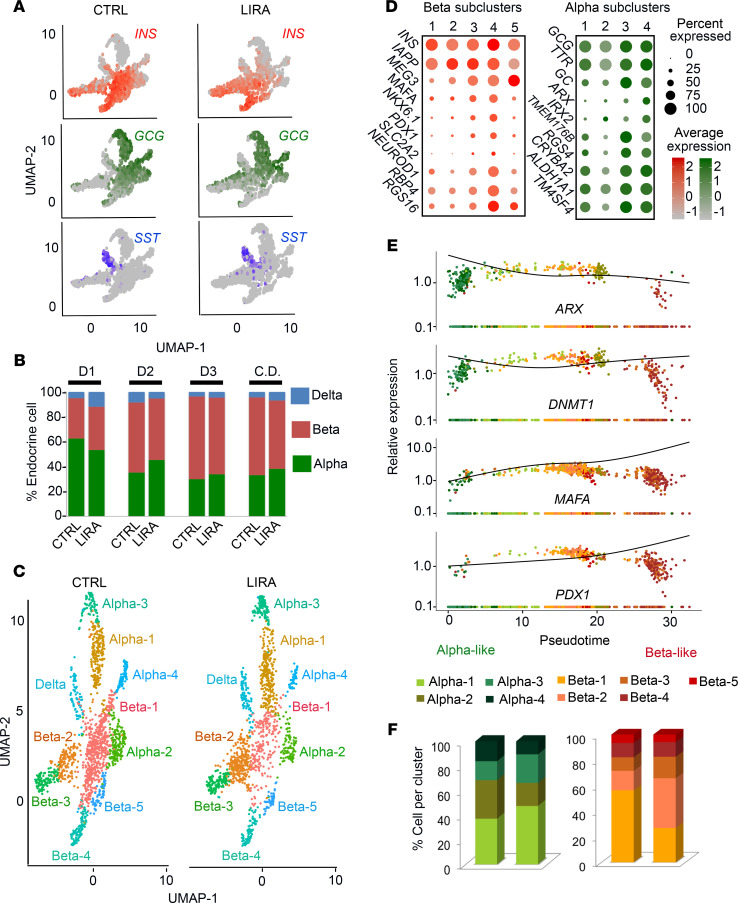
图三
假时间轨迹分析显示,α细胞亚群在利拉鲁肽处理后表现出向β细胞特征转变的趋势,特别是α-1亚群中PCSK1、INS和IAPP的表达显著增加(图3D和3E)。
活性GLP-1测量:
 图五
图五
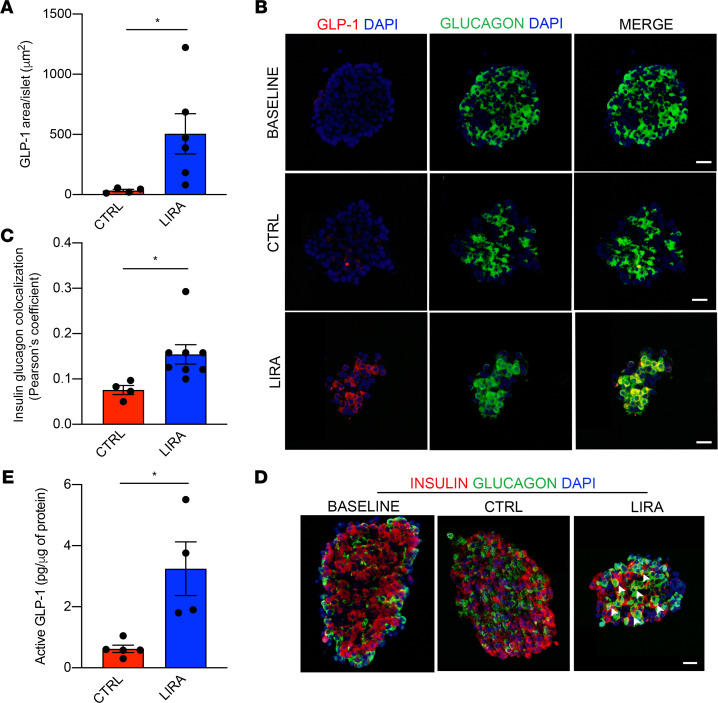
研究发现,利拉鲁肽处理显著增加了人类胰岛中活性GLP-1的含量,证实了α细胞在GLP-1R激动剂作用下能够产生具有生物活性的GLP-1(图5E)。
β细胞GLP-1R信号增加双激素表达的胰岛细胞
小鼠模型实验:
利拉鲁肽处理显著增加了WT小鼠胰岛中双激素表达的胰岛细胞(即同时表达胰岛素和胰高血糖素的细胞)的比例,而在KO小鼠中未观察到这一现象(图6A和6B)。
进一步分析显示,这些双激素细胞主要分布在胰岛的外围区域,表明β细胞GLP-1R信号通过旁分泌机制影响α细胞。
人类胰岛验证:
免疫组化分析显示,利拉鲁肽处理显著增加了人类胰岛中GLP-1+和双激素表达的细胞数量(图5A至5D)。
讨论
本研究揭示了GLP-1R激动剂通过β细胞GLP-1R信号增强α细胞PCSK1和GLP-1表达的新机制。这些发现不仅为理解GLP-1在胰岛功能调节中的作用提供了新的视角,还为开发针对α细胞GLP-1生产的糖尿病治疗新策略提供了理论依据。通过DART-Seq技术,研究团队验证了一种高灵敏度的单细胞RNA测序方法,为未来胰岛细胞功能研究提供了重要的工具。
结论
研究结果表明,β细胞GLP-1R信号通过增强α细胞PCSK1表达,促进GLP-1的产生,并诱导α细胞向β细胞样细胞转变。这一过程可能通过旁分泌机制实现,涉及β细胞分泌的特定因子。这些发现为开发新型糖尿病治疗策略提供了潜在的靶点,并强调了GLP-1R激动剂在调节胰岛细胞功能中的重要作用。
方法学细节和关键图表
动物实验设计(图1A):
8周龄的雄性和雌性小鼠接受高脂饮食(HFD)6周,随后转为含tamoxifen的HFD饮食,以诱导β细胞GLP-1R敲除。
小鼠接受利拉鲁肽(200 μg/kg)或生理盐水处理2周后,收集组织样本进行分析。
DART-Seq技术(图2A至2C):
DART-Seq通过在DROP-Seq的基础上增加特定探针,显著提高了对低丰度转录本(如PCSK1)的检测灵敏度。
与DROP-Seq相比,DART-Seq在检测PCSK1表达方面表现出更高的信号强度和单细胞分辨率。
单细胞转录组分析(图3D和3E):
假时间轨迹分析显示,α细胞亚群在利拉鲁肽处理后表现出向β细胞特征转变的趋势,特别是α-1亚群中PCSK1、INS和IAPP的表达显著增加。
活性GLP-1测量(图5E):
利拉鲁肽处理显著增加了人类胰岛中活性GLP-1的含量,证实了α细胞在GLP-1R激动剂作用下能够产生具有生物活性的GLP-1。
图六
双激素表达的胰岛细胞分析(图6A和6B):
利拉鲁肽处理显著增加了WT小鼠胰岛中双激素表达的胰岛细胞的比例,而在KO小鼠中未观察到这一现象。
| 名称 | 货号 | 规格 |
| V-PLEX GLP-1 Active Kit , SECTOR (1 PL) | K1503OD-1 | 1PL |
| V-PLEX Vascular Injury Panel 2(human) Kit (5 Plate) | K15198D-2 | 5Plate |
| V-PLEX Vascular Injury Panel 2(human) Kit (1 Plate) | K15198D-1 | 1Plate |