Forsythoside A Mitigates Alzheimer's-like Pathology by Inhibiting Ferroptosis-mediated Neuroinflammation via Nrf2/GPX4 Axis Activation
引言
阿尔茨海默病(Alzheimer's Disease, AD),作为一种严重的神经退行性疾病,日益成为全球公共卫生的重大挑战。其复杂的病理机制涉及多个生物过程,其中铁死亡(ferroptosis)和神经炎症被证实为核心环节。福斯科苷A(Forsythoside A, FA),源自传统中药材连翘的主要成分,近年来因其显著的抗炎、抗氧化和神经保护作用而受到广泛关注。本研究深入探讨了FA在AD病理中的作用机制,特别是在调节铁死亡介导的神经炎症方面,为AD的治疗提供了新的视角和潜在的药物靶点。

研究背景与目的
AD的主要特征是大脑内β-淀粉样蛋白(Aβ)沉积和神经纤维缠结,导致神经元功能逐渐丧失,引发记忆和认知能力的严重衰退。铁死亡作为一种铁依赖的细胞死亡形式,与脂质过氧化、线粒体功能障碍等密切相关,近年来被发现在AD病理进程中扮演重要角色。同时,神经炎症作为AD的另一大病理特征,涉及多种炎症因子和信号通路的激活,进一步加剧了神经元的损伤。
FA作为一种天然化合物,已被证明具有多种生物活性,包括抗炎、抗氧化和神经保护等。本研究旨在深入探究FA对AD病理的影响,特别是其在抑制铁死亡介导的神经炎症方面的作用机制,以期为AD的治疗提供新的策略。
材料与方法
实验对象与分组
本研究采用了多种实验模型,包括APP/PS1双转基因AD小鼠、Aβ1-42诱导的N2a细胞、erastin刺激的HT22细胞以及LPS诱导的BV2细胞,以全面评估FA在AD病理中的作用。实验动物和细胞均经过严格筛选和分组,确保实验结果的准确性和可靠性。
药物处理与观察指标
FA以不同浓度和时间点处理实验对象,通过观察细胞活力、脂质过氧化水平、炎症因子分泌等关键指标,评估FA对铁死亡和神经炎症的影响。同时,利用蛋白质组学、免疫组化、酶联免疫吸附试验(ELISA)和蛋白质印迹(Western blot)等技术手段,深入探究FA作用的具体机制。
实验结果与分析
FA改善线粒体功能并抑制脂质过氧化
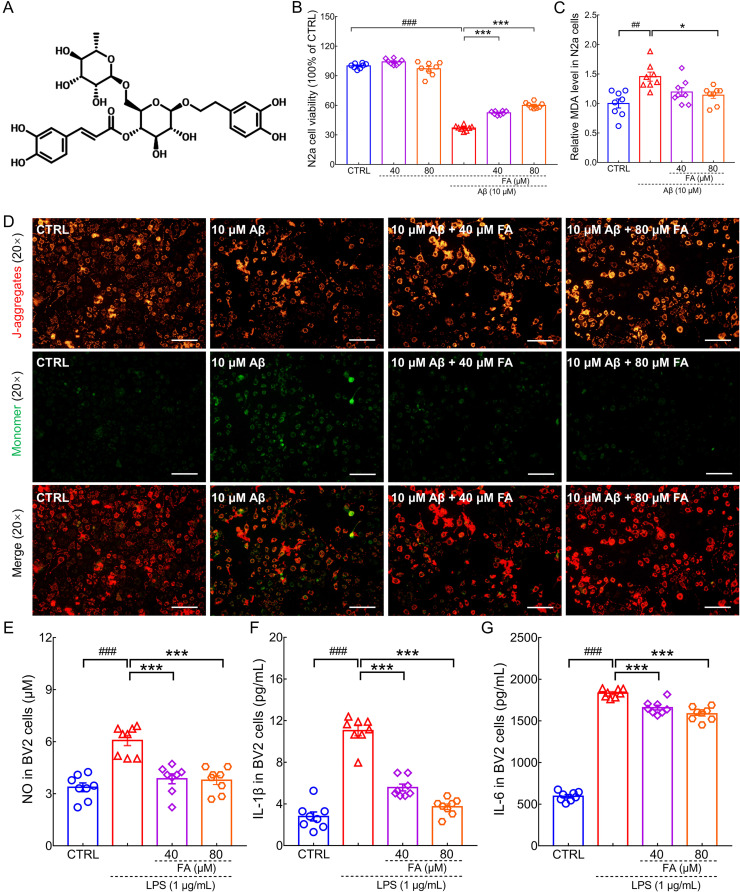
在Aβ1-42诱导的N2a细胞中,FA处理显著改善了线粒体的功能,降低了脂质过氧化水平,表明FA具有抑制铁死亡的作用。这一发现为FA在AD治疗中的潜力提供了初步证据。
FA抑制神经炎症因子的产生
在LPS刺激的BV2细胞中,FA处理显著降低了IL-6、IL-1β和NO等炎症因子的产生,表明FA具有显著的抗炎作用。这一发现进一步支持了FA在AD治疗中的潜在价值,因为神经炎症是AD病理进程中的重要因素。
FA改善APP/PS1小鼠的记忆和认知功能
在APP/PS1双转基因AD小鼠中,FA处理显著改善了小鼠的记忆和认知功能,降低了大脑中的Aβ沉积和p-tau水平。这一发现不仅证实了FA在AD模型中的有效性,还为其作用机制的研究提供了重要的实验依据。
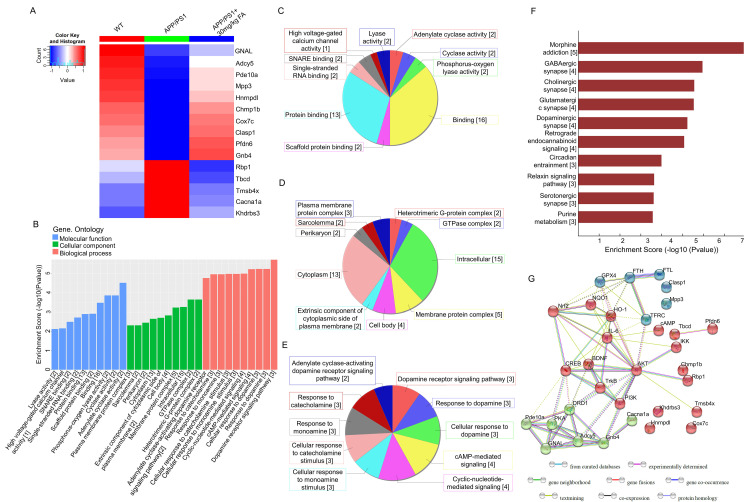
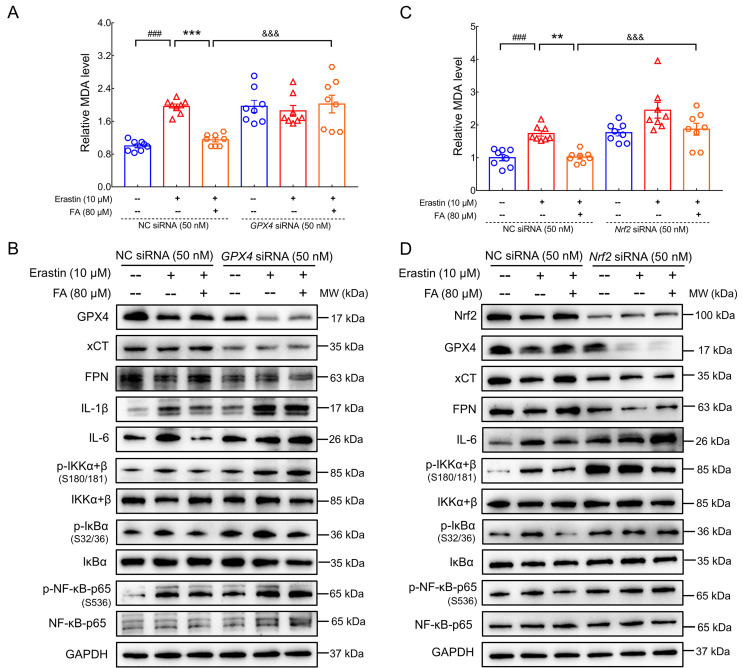
FA通过Nrf2/GPX4轴抑制铁死亡介导的神经炎症
进一步的研究发现,FA通过激活Nrf2/GPX4轴,抑制了铁死亡介导的神经炎症。Nrf2作为一种重要的抗氧化应激调节因子,能够诱导抗氧化酶的表达,从而保护细胞免受氧化应激的损伤。GPX4作为谷胱甘肽过氧化物酶家族的成员,具有清除脂质过氧化物的功能,是铁死亡的关键抑制因子。FA通过激活Nrf2/GPX4轴,上调了GPX4的表达,从而降低了脂质过氧化水平,抑制了铁死亡的发生。同时,FA还抑制了IKK/IκB/NF-κB信号通路的激活,减少了炎症因子的分泌,进一步抑制了神经炎症的发生。
FA促进抗炎症因子的产生
除了抑制炎症因子的产生外,FA还促进了抗炎症因子的产生,如IL-10和TGF-β等。这些抗炎症因子能够抑制炎症反应的进一步加剧,促进神经元的修复和再生,从而进一步改善AD的病理改变。
讨论与展望
本研究首次揭示了FA通过激活Nrf2/GPX4轴抑制铁死亡介导的神经炎症以减轻AD样病理改变的机制。这一发现不仅为AD的治疗提供了新的策略,还为FA作为潜在药物成分的开发提供了理论依据。
FA的潜在临床应用价值
FA作为一种天然化合物,具有低毒性、高生物利用度等优点,有望成为AD治疗的新药物。未来的研究可以进一步探索FA在AD患者中的安全性和有效性,为其临床应用提供更有力的证据。
深入研究FA的作用机制
虽然本研究已经揭示了FA抑制铁死亡介导的神经炎症的部分机制,但仍有许多未知领域等待探索。例如,FA如何具体调节Nrf2/GPX4轴的活性?FA是否还通过其他途径影响AD的病理进程?这些问题的解答将有助于更全面地理解FA在AD治疗中的作用机制。
拓展FA的应用范围
除了AD外,FA还可能对其他神经退行性疾病具有治疗作用。未来的研究可以探索FA在其他神经退行性疾病中的潜在应用价值,为其临床应用提供新的思路。
结论
综上所述,本研究通过一系列实验模型和技术手段,深入探讨了FA在AD病理中的作用机制。研究发现,FA通过激活Nrf2/GPX4轴抑制铁死亡介导的神经炎症,从而减轻AD样病理改变。这一发现为AD的治疗提供了新的策略和潜在药物靶点。未来的研究可以进一步探索FA在AD患者中的安全性和有效性,并拓展其应用范围至其他神经退行性疾病的治疗中。
| 名称 | 货号 | 规格 |
| N-Cadherin (D4R1H) XP ® Rabbit mAb | 13116T | 20ul |
| N-Cadherin (D4R1H) XP ® Rabbit mAb | 13116S | 100ul |
| SMAD2/3 (D7G7) XP ® Rabbit mAb | 8685S | 100ul |
| Rabbit anti-Phospho-Smad2/3(Thr8) Polyclonal Antibody | abs130992-100ug | 100ug |